NaClO2的漂白能力是漂白粉的4~5倍, NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下: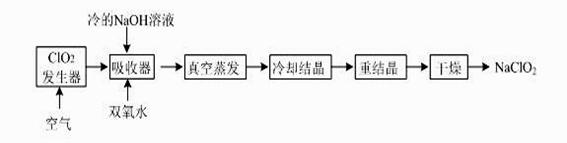
(1)ClO2发生器中的反应为: NaClO3+SO2+H2SO4→ClO2+NaHSO4(未配平),该反应中氧化剂与还原剂的物质的量之比为_________,实际工业生产中,可用硫黄、浓硫酸代替原料中的SO2,其原因为__________(用化学方程式表示)。
(2)反应结束后,向ClO2发生器中通入一定量空气的目的:__________。
(3)吸收器中生成NaClO2的离子反应方程式为__________。
(4)某化学兴趣小组用如下图所示装置制备SO2并探究SO2与Na2O2的反应:
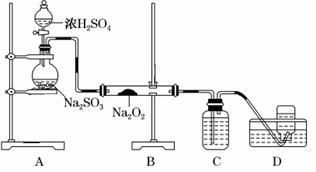
①盛放浓H2SO4仪器名称为__________。
②A装置用于实验室制取SO2,发生反应的化学方程式为。
③D中收集到的气体可使带余烬的木条复燃,B中发生的反应可能为__________、Na2O2+SO2![]() Na2SO4。
Na2SO4。
答案
答案:(1)S+2H2SO4(浓) ![]() 3SO2↑+ 2H2O
3SO2↑+ 2H2O
(2)驱赶出ClO2,确保其被充分吸收
(3)2ClO2+2OH-+H2O2![]() 2ClO2-+O2+2H2O
2ClO2-+O2+2H2O
(4)分液漏斗;Na2SO3+H2SO4(浓) ![]() Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
2Na2O2+2SO2![]() 2Na2SO3+O2
2Na2SO3+O2


