主族元素W、X、Y、Z的原子序数依次增大,且均不大于20。Y元素原子的最外层电子 数是内层电子数的3倍,Z元素原子的最外层电子数是最内层电子数的一半。甲是W、X两种元素形成的简单化合物,水溶液呈碱性,乙是Y元素的单质。在工业生产中它们有如下转化关系。下列叙述正确的是
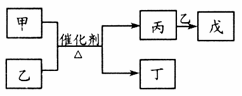

A.原子半径的大小W<X<Y<Z
B.戊与丁反应过程中氧化剂与还原剂的物质的量之比为1:2
C.Y与Z形成的所有化合物中只存在离子键
D.X元素的氧化物对应的水化物均为强酸
答案
【答案】B
【解析】据原子序数增大的要求,由Y、Z原子结构特征可知分别是氧、钠(或钾)元素;又由甲的组成和性质可知其为NH3,则W、X分别是氢、氮元素;Y元素的单质乙通常为O2;最后由转化关系得丙、丁、戊分别是NO、H2O、NO2。前20号元素中,原子最外层电子数是内层电子数的3倍的元素是氧,原子最外层电子数是最内层电子数的一半的元素有锂、钠、钾,Y的原子序数小于Z,则Y为氧(O)、Z为钠(Na)或钾(K)。简单化合物甲的水溶液呈碱性,甲只能是氨(NH3),则W、X元素分别是氢(H)、氮(N)。Y元素的单质乙通常是O2。据物质转化关系图,丙、丁、戊分别是NO、H2O、NO2。A项:据周期表中主族元素原子半径变化规律,得原子半径H<O<N<Na(或K),A项错误;B项:戊与丁反应3NO2+H2O=2HNO3+NO中,NO2得电子生成NO,NO2是氧化剂,2NO2失电子生成HNO3,2NO2是还原剂,氧化剂与还原剂物质的量之比为1:2,B项正确;C项:Y与Z形成的化合物有Na2O、Na2O2、K2O等,其中Na2O2有离子键和共价键,C项错误;D项:X元素的氧化物对应的水化物有HNO3、HNO2,其中HNO3为强酸,HNO2属于弱酸,D项错误。
