向20 mL HCl和H2SO4的混合溶液中逐滴加入0.1 mol·L-1的Ba(OH)2溶液,生成沉淀的质量和溶液的pH与加入的Ba(OH)2溶液体积的关系如图5所示。试完成下列问题:
 图5
图5
(1)起始时,混合酸中硫酸的物质的量浓度为______________ mol·L-1。
(2)起始时,混合酸中盐酸的物质的量浓度为______________ mol·L-1。
(3)B点表示的沉淀的质量为______________g。
(4)A点表示溶液中的c(H+)为______________ mol·L-1,pH为______________。
(5)C点的pH为______________(pH可直接用对数表示)。
答案
【答案】0.10.40.4660.2071.18或-lg![]()
 (4)A点表示溶液中硫酸恰好被完全中和,溶质是HCl,c(H+)=
(4)A点表示溶液中硫酸恰好被完全中和,溶质是HCl,c(H+)=![]() ;pH=
;pH= ![]() ;(5)C点的溶液表示盐酸中的氢离子被中和了一半。C点溶液中c(H+)=
;(5)C点的溶液表示盐酸中的氢离子被中和了一半。C点溶液中c(H+)=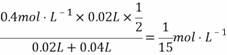 ;pH=
;pH= ![]() 。
。

