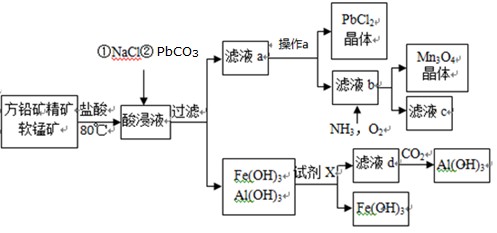
四氧化三锰(Mn3O4)是电子工业的磁性材料,而氯化铅(PbCl2)常用于焊料和助溶剂、制备 其他铅盐等。现用 34.375kg 方铅矿精矿(主要成分为 PbS)和软锰矿(主要成分是 MnO2,还含有 Fe2O3、 Al2O3 等杂质)样品,制备 PbCl2 和 Mn3O4 的工艺流程如下:
已知:PbCl2(s) + 2Cl-(aq) PbCl2
( aq) ΔH > 0
![]() -
-
4
(1)80℃时,为提高方铅矿精矿、软锰矿与盐酸反应的速率,可采取的措施有 (写出一条即可)。 (2)试剂 X 是 (填“化学式”)。
(3)用盐酸处理两种矿石粉末,生成等物质的量的 MnCl2、PbCl2 和 S 的总反应化学方程式为 。
(4)操作 a 的方法: 、冷却结晶、过滤、洗涤、干燥。
(5)向滤液 b 中通入 NH3 和 O2 发生反应后,总反应的离子方程式为 。
(6)金属锰可以用 Mn3O4 为原料,通过铝热反应来制备。当消耗金属铝的质量为 2.4kg 时,原样品中含 锰的质量分数为(假设过程中无损耗) (用百分数表示)。
答案
.(每空 2 分,共 12 分) (1)粉碎矿石、搅拌、适当增大盐酸浓度等 (2)NaOH(或 KOH 等强碱均可)
![]() 80℃
80℃
(3) MnO2+PbS+4HCl======MnCl2+PbCl2+S+2H2O (反应条件错了扣 1 分,未配平不得分)
(4)蒸发浓缩
(5)6Mn2++12NH3+6H2O+O2 12NH
+2Mn O ↓(反应条件错了扣 1 分,未配平不得分)
(6)16%
+
![]() 4 3 4
4 3 4

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L