磷在于人体所有细胞中,是维持骨骼和牙齿牙的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为 ,有 个未成对电子。
(2)磷的一种同素异形体——白磷(P4)的立体构型为 ,其键角为 ,推测其在CS2中的溶解度 (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析 PH3的键角小于NH3的原因 。
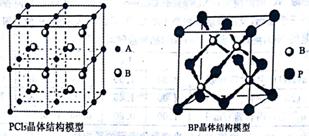
(4)常温下PC15是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与 CC14、SF6互为等电子体,则A为 ,其中心原子杂化轨道类型为 ,B为 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点 (填“高于”或“低于”)金刚石熔点。已知其B—P键长均为x cm,则其密度为 g/cm3(列出计算式即可)。
答案
(1)1s22p63s23p3;3
(2)正四面体形;60°;大于
(3)电负性N强于P,中心原子的电负性越大,成键电子对离中心原子越近,成键电子对之间距离越小,成键电子对之间的排斥力增大,键角变大。(2分)
(4) PCl4+;sp3;PCl6-
(5)低于;![]() 或
或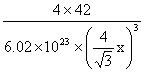 (3分)
(3分)
