下列说法错误的是( )
A.常温下,pH相等的①NaHCO3、②Na2CO3、③NaOH溶液的物质的量浓度大小为③<②<①
B.25℃时,PH=10的NaOH溶液和PH=10的Na2CO3溶液中水的电离程度相同
C.常温下,若测得NaHA溶液的PH>7,则该溶液中一定有c(H2A)> c(A2-)
D.0.1mol/LNa2CO3溶液与0.1mol/L NaHCO3溶液等体积混合,该溶液中的各离子浓度符合此关系:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+)
答案
【答案】B
【解析】A.碳酸钠的水解程度大于碳酸氢钠,则常温下,pH相等的①NaHCO3、②Na2CO3、③NaOH溶液的物质的量浓度大小为③<②<①,A正确;B.NaOH抑制水的电离,Na2CO3溶液中碳酸根水解,促进水的电离,B错误;C.常温下,若测得NaHA溶液的pH>7,这说明HA-的水解程度大于电离程度,因此该溶液中一定有c(H2A)>c(A2-),C正确;D.0.1mol/LNa2CO3溶液与0.1mol/L NaHCO3溶液等体积混合,根据物料守恒可知该溶液中的各离子浓度符合此关系:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+),D正确,答案选B。
【点睛】准确判断溶液中存在的微粒以及相应的平衡是解答的关键,注意电荷守恒、物料守恒的灵活应用。另外要注意掌握离子浓度大小比较的一般解题思路,归纳如下: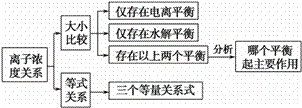 。
。

 NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。
NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。