人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
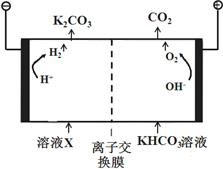 (1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,
(1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,
再利用电解法使K2CO3溶液再生,其装置如图所示。
在阳极区发![]() 生的反应包括
生的反应包括
和H ++HCO3-=H2O + CO2↑。简述CO32-在阴极区再生的
原理 。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲
醇等产物,工业上利用该反应合成甲醇。已知:25 ℃,101 KPa下: H2(g)+1/2O2(g)=H2O(g) ΔH1= -242 kJ/mol;CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH2=-676 kJ/mol;写出CO2和H2生成气态甲醇等产物的热化学方程式 。
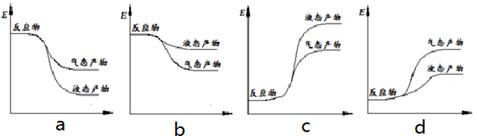
下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。
 |
 (3)在密闭的再生装置中,加入5 mol H2与2 mol CO2发
(3)在密闭的再生装置中,加入5 mol H2与2 mol CO2发
生反应生成甲醇,反应达到平衡时,改变温度(T)和
压强(P),反应混合物中甲醇(CH3OH)的物质的量分
数变化情况如图所示,下列说法正确的是( )
A.P1> P2> P3>P4
B.甲醇的物质的量分数越高,反应的平衡常数越大
 C.图示中,该反应的温度变化为:T1> T2> T3>T4
C.图示中,该反应的温度变化为:T1> T2> T3>T4
D.T4、P4、时,H2的平衡转化率为60%
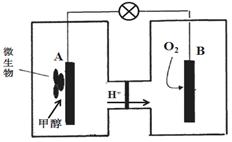
(4)已知某种甲醇燃料电池中,电解质溶液为酸性,如图
所示。工作结束后,B电极室溶液的pH与工作前相
比将 (填“增大、减小或不变”,溶液体积变
化忽略不计)。
答案
(1)4OH–-4e–= 2H2O+O2↑(或2H2O-4e–=4H+ + O2↑)(2分);
HCO3–存在电离平衡:HCO3–![]() H++CO32-,阴极H+放电,浓度减小平衡右移(或溶液中H+放电,增大了OH –浓度,与HCO3 –反应,从而使CO32-再生)(2分)
H++CO32-,阴极H+放电,浓度减小平衡右移(或溶液中H+放电,增大了OH –浓度,与HCO3 –反应,从而使CO32-再生)(2分)
(2)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH =-50 kJ/mol(2分);a(1分)
(3)ACD(2分) (4)不变(1分)
