浓度均为0.1 mol·L-1、体积均为V0的HX、HY溶液,分别加水稀释至体积V,pH随lg![]() 的变化关系如下图所示。下列叙述正确的是( )
的变化关系如下图所示。下列叙述正确的是( )
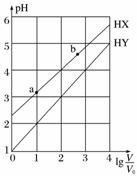
A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.常温下,由水电离出的c(H+)·c(OH-):a<b
C.相同温度下,电离常数K(HX):a>b
D.lg![]() =3,若同时微热两种溶液(不考虑HX 、HY和H2O的挥发),则
=3,若同时微热两种溶液(不考虑HX 、HY和H2O的挥发),则![]() 减小
减小
答案
答案 B
解析 A项,根据图分析,当lg![]() =0,HX的pH>1,说明HX部分电离,为弱电解质,HY的pH=1,说明其完全电离,为强电解质,所以HY的酸性大于HX,错误,不选A;B项,酸或碱抑制水的电离,酸中的氢离子浓度越小,其抑制水电离程度越小,根据图分析,b溶液中氢离子浓度小于a,则水的电离程度a<b,所以由水电离出的氢离子和氢氧根离子浓度的乘积a<b,正确,选B;C项,酸的电离平衡常数只与温度有关,所以相同的温度下,电离常数a=b,错误,不选C;D项,lg
=0,HX的pH>1,说明HX部分电离,为弱电解质,HY的pH=1,说明其完全电离,为强电解质,所以HY的酸性大于HX,错误,不选A;B项,酸或碱抑制水的电离,酸中的氢离子浓度越小,其抑制水电离程度越小,根据图分析,b溶液中氢离子浓度小于a,则水的电离程度a<b,所以由水电离出的氢离子和氢氧根离子浓度的乘积a<b,正确,选B;C项,酸的电离平衡常数只与温度有关,所以相同的温度下,电离常数a=b,错误,不选C;D项,lg![]() =3,若同时微热两种溶液,X-物质的量增多,Y-物质的量不变,二者溶液的体积相等,所以
=3,若同时微热两种溶液,X-物质的量增多,Y-物质的量不变,二者溶液的体积相等,所以![]() 比值变大,错误,不选D。
比值变大,错误,不选D。

 NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。
NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。