同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知
P4(s,白鳞)+5O2(g)=P4O10(s);△H=-2983.2 kJ/mol ①
P(s,红磷)+![]() O2(g)=
O2(g)=![]() P4O10(s);△H=-738.5 kJ/mol ②
P4O10(s);△H=-738.5 kJ/mol ②
则白磷转化为红磷的热化学方程式为 。相同状况下,能量状态较低的是 ;白磷的稳定性比红磷 (填“高”或“低”)。
![]() P4(S,白磷)=P(S,红磷) △H=-7.3 kJ·mol-1 红磷 低
P4(S,白磷)=P(S,红磷) △H=-7.3 kJ·mol-1 红磷 低
根据图示,写出反应的热化学方程式。
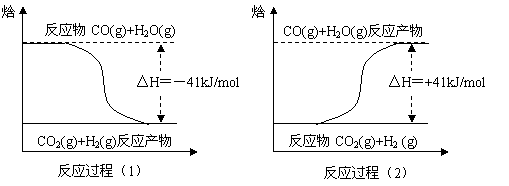 |
(1)的热化学方程式为
(2)的热化学方程式为
(1)CO(g)+2H2O(g)=CO2(g)+H2(g) △H=-41 kJ·mol-1
(2)CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41 kJ·mol-1
0.3mol气态高能燃料乙硼烷(分子式B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量,则其热化学方程式为 。又已知H2O(l)=H2O(g) △H=44 kJ·mol-1,则11.2L标准状况下的乙硼烷完全燃烧生成气态水时放出的热量是 kJ。
B2H5(g)+3O2(g)=B2O3(s)+2H2O(l) △H=-2165 kJ·mol-1 1016.5
若2.6g乙炔(气态)完全燃烧生成液态水和CO2(气态)时放热130kJ,则乙炔燃烧的热化学方程式为 。
C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) △H=-1300 kJ·mol-1
O2(g)=2CO2(g)+H2O(l) △H=-1300 kJ·mol-1
下列说法中,正确的是( )
A.在化学反应中发生物质变化的同时,不一定发生能量变化
B.△H>0表示放热反应,△H<0表示吸热反应
C.△H的大小与热化学方程式中计量数无关
D.当生成物释放的总能量大于反应物吸收的总能量时,△H<0
D
本卷还有10题,登录并加入会员即可免费使用哦~

该作品由: 用户明高人分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。