9.2 g金属钠投入到足量的重水中,则产生的气体中含有 ( )
A.0.2 mol中子 B.0.4 mol电子
C.0.2 mol质子 D.0.4 mol分子
解析 n(Na)=![]() =0.4 mol
=0.4 mol
Na与重水反应的化学方程式为
2Na+2D2O===2NaOD+D2↑
2 1
0.4 mol 0.2 mol
由方程式可知生成D2气体0.2 mol,所以气体中含中子0.4 mol,含电子0.4 mol,含质子0.4 mol,含分子0.2 mol,故B正确。
答案 B
除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是 ( )
A.通入二氧化碳气体 B.加入氢氧化钡溶液
C.加入澄清石灰水 D.加入稀盐酸
解析 除杂方法要操作简便、效果好、不带来新的杂质、保留非杂质成份。溶液中可用这样的方法: Na2CO3 + H2O + CO2===2NaHCO3。
答案 A
25℃时,浓度均为0.2 mol/L的NaHCO3与Na2CO3溶液中,下列判断不正确的是 ( )
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.c(OH-)前者大于后者
D.分别加入NaOH固体,恢复到原温度,c(CO![]() )均增大
)均增大
解析 在NaHCO3溶液中HCO![]() 作为弱酸的酸式酸根既能电离也能水解,同时还存在水的电离平衡;在Na2CO3溶液中存在CO
作为弱酸的酸式酸根既能电离也能水解,同时还存在水的电离平衡;在Na2CO3溶液中存在CO![]() 的水解平衡和水的电离平衡,A项正确;在两溶液中均存在Na+、H+、CO
的水解平衡和水的电离平衡,A项正确;在两溶液中均存在Na+、H+、CO![]() 、HCO
、HCO![]() 、H2CO3、OH-、H2O七种微粒,B项正确;同浓度的正盐水解程度大于其酸式盐,所以Na2CO3溶液中c(OH-)大,碱性强,C项错;D选项中,NaHCO3溶液中NaHCO3+NaOH===Na2CO3+H2O,使c(CO
、H2CO3、OH-、H2O七种微粒,B项正确;同浓度的正盐水解程度大于其酸式盐,所以Na2CO3溶液中c(OH-)大,碱性强,C项错;D选项中,NaHCO3溶液中NaHCO3+NaOH===Na2CO3+H2O,使c(CO![]() )增大,在Na2CO3溶液中加入NaOH固体抑制了CO
)增大,在Na2CO3溶液中加入NaOH固体抑制了CO![]() 的水解,使c(CO
的水解,使c(CO![]() )增大,D正确。
)增大,D正确。
答案 C
下列叙述中正确的是 ( )
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2CO3饱和溶液中通入足量CO2,有NaHCO3结晶析出
解析 CaCO3+CO2+H2O===Ca(HCO3)2,前半句正确,加入NaHCO3饱和溶液后,没有沉淀产生,A错误;向Na2CO3溶液中滴加等物质的量的稀盐酸,发生反应为Na2CO3+HCl===NaCl+NaHCO3,没有CO2生成,B错误;等质量的NaHCO3和Na2CO3,与足量盐酸反应,产生的CO2体积不同,NaHCO3生成的CO2更多些,C错误;溶解度:Na2CO3>NaHCO3,向Na2CO3饱和溶液中通入足量CO2后溶液中有NaHCO3晶体析出,D正确。
答案 D
为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g样品加热,其质量变为w2 g,则该样品的纯度(质量分数)是 ( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
解析 样品加热发生反应为:
2NaHCO3△,Na2CO3+H2O+CO2↑ Δm
168 106 62
m(NaHCO3) w1-w2
质量差为w1-w2,故样品中NaHCO3质量为:![]() g,Na2CO3质量为w1 g-
g,Na2CO3质量为w1 g-![]() g,其纯度(质量分数)为
g,其纯度(质量分数)为![]() =
=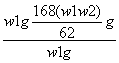 =
=![]() 。
。
答案 A
本卷还有9题,登录并加入会员即可免费使用哦~

该作品由: 用户通天教主分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。