由新型无机非金属材料制成的无水冷发动机,热效率高、寿命长。这类材料中研究较多的是化合物G。
(1)化合物G的相对分子质量为140,G中含硅元素,其质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:G和E的化学式分别为 、 。
(2)粉末状G能够与氧气反应,所得产物中有一种是空气中的主要成分,另一种是工业上生产玻璃的主要原料。请写出化合物G与氧气反应的化学方程式 。
(3)常压下在G中添加氧化铝,经高温烧结可制制成一种高强度、超硬度、耐磨损、
抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-XAlXOXY8-X。在接近1700℃时x的极限值约为4.0,在1400℃时x为2.0,以保持整个化合物呈电中性。推测:赛伦中以下元素的化合价:Si ,Y ,塞伦的晶体类型 。
【解析】该题涉及到元素及其化合物,新型材料,晶体的性质等综合知识的考查.
G中含硅和氮。其中含Si:140×60%÷28=84÷28=3 N:140×40%÷14=4
故G的化学式为:Si3N4 E的化学式为:SiC14
G与O2反应的化学方程式为:Si3N4+3O2=3SiO2+2N2
原子晶体具有高强度、超硬度、耐磨损、抗腐蚀等特性。
【答案】(1)Si3N4、SiC14;
(2)Si3N4+3O2=3SiO2+2N2;
(3)+4,-3 原子晶体
Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)![]() 2C(g);反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g);反应达到平衡后,再恢复至原温度。回答下列问题:
(1)可根据 现象来判断甲、乙都已达到平衡。
(2)达到平衡时,隔板K最终停留在0刻度左侧a处,
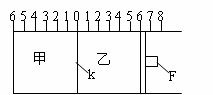
则a的取值范围是 (3)若达到平衡时,隔板K最终停留在左侧刻度1处,则甲中C的物质的量为 mol,乙中C的转化率 ______50%(填:>、<、=),此时,乙中可移动活塞F最终停留在右侧刻度 处(填下列序号)① <6 ② >6 ③ =6。
(4)若达到平衡时,隔板K最终停留在左侧刻度靠近0处,则乙中可移动活塞F最终停留在右侧的刻度不大于 ;若K最终停留在左侧刻度靠近2处,则乙中F最终停留在右侧的刻度不小于 。
(Ⅱ)若一开始就将K、F固定,其他条件均不变,则达到平衡时:
(1)甲、乙中C的摩尔分数是 (填:“甲>乙”或“甲<乙”或“甲=乙” );
(2)测得甲中A的转化率为b,则乙中C的转化率为 ;
(3)假设乙、甲两容器中的压强比用d表示,则d的取值范围是 。
【解析】该题涉及化学反应速率和化学反应限度的有关问题的讨论和化学平衡移动原理的应用,是近几年高考中常考的题型之一。
【答案】(Ⅰ)(1)K、F不再移动
(2)0<a<2
(3)1 > ② (4)8 4
(Ⅱ)(1)甲=乙 (2)1-b (3)![]() <d<
<d<![]()
某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意图如下:
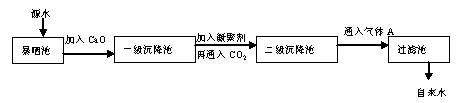
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后生成Ca(OH)2,进而发生若干复分解反应,试写出其中的一个离子方程式
。
(2)加入凝聚剂可以除去其中的悬浮固体颗粒,其过程是 。
(填写下列各项的序号)
①只有物理过程,无化学过程
②只有化学过程,无物理过程
③既有化学过程又有物理过程
FeSO4・7H2O是常用的凝聚剂,加入后,最终生成红褐色胶状沉淀,则这种红褐色胶状沉淀是 。
(3)通入二氧化碳的目的是
和
(4)气体A的作用是 。
(5)下列物质中, 可以作为气体A的代替品。(填写下列各项的序号)
①ClO2 ②浓氨水 ③SO2 ④浓硫酸
【解析】联系化工生产与生活实际的题型是高考常考的题型之一,污水的处理尤其重要。
【答案】(1)只要写出下列4个离子方程式中的任意一个,即可给2分。
HCO-3+OH- CO2-3+H2O; Ca2++CO32- CaCO3↓;
Ca2++2HCO-3+2OH- CaCO3↓+CO32-+2H2O;
Mg2++2OH- Mg(OH)2↓
(2)③;Fe(OH)3
(3)除去钙离子;调节溶液酸度
(4)杀菌消毒或氧化性
(5)①
A、B、C、D均为中学常见的物质,它们间的反应关系如下图所示:
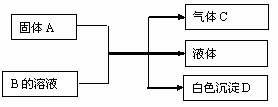
(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式为____________。
有关反应的化学方程式为___________________ ___________________________。
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液。
① A是NaHCO3时,该反应的离子方程式为:
_____________________________________________________。
② A是一种淡黄色的固体,且A和B以物质的量之比为2:1混合时,推知B的
化学式_________________。
(3)若A是碳化钙(CaC2),A与B的溶液反应时只生成C、CaCO3和水;C的燃烧热为1300 kJ・mol-1,则B得化学式为_______________;
【解析】这是以元素及其化合物为背景,涉及物质的分类方法,简单的、常规的计算,知识面比较宽。主要考查对常见化合物的性质掌握理解能力。
【答案】⑴(NH4)2SO4 (NH4)2SO4+Ba(OH)2=BaSO4↓+2NH3↑+2H2O
⑵① Al3++3HCO3-=Al(OH)3↓+3CO2↑
②Al2(SO4)3
⑶ Ca(HCO3)2 2C2H2 (g)+5O2(g)===4CO2(g)+2H2O(l);Δ H =-2600 kJ・mol-1
工业上生产氯气,常用在电解槽中电解饱和食盐水的方法,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分。下图(左图)为电解槽的示意图。
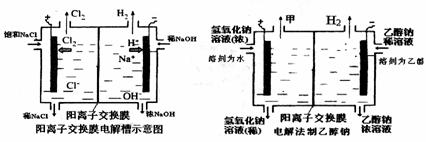
(1)这种阳离子交换膜,只允许溶液中的 通过。(填下列微粒的编号)
①H2 ②Cl2 ③H+ ④Cl- ⑤Na+ ⑥OH-
(2)写出在电解过程中发生的电极方程式
阳极: 。
(3)已知某电解槽每小时加入10%的氢氧化钠溶液10kg,每小时能收集到标况下的氢气896L,而且两边的水不能自由流通。则理论上计算,电解后流出的氢氧化钠溶液的质量分数为 。
(4)某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如上右图所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇。回答下列问题:
①写出在电解过程中发生的电极方程式
阴极: 。
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇固体的方法是: 。
【答案】③⑤(2)阳极;2Cl--2e-=Cl2
(3)35.7%
(4)①阴极:2CH3CH2OH+2e-=2CH3CH2O-+H2
②蒸发结晶
本卷还有6题,登录并加入会员即可免费使用哦~

该作品由: 用户abc分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。