X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子.则这四种金属的活动性由强到弱的顺序为
A X>Z>Y>M B X>Y>Z>M C M>Z>X>Y D X>Z>M>Y
A
用惰性电极电解某溶液时,发现两极只有H2和O2生成,则电解一段时间后,若电解前后温度变化忽略不计,下列有关溶液叙述正确的有
①该溶液的pH可能增大 ②该溶液的pH可能减小 ③该溶液的pH可能不变
④该溶液的浓度可能增大 ⑤该溶液的浓度可能不变
A.①②③④⑤ B.只有①②④⑤
C.只有①③⑤ D.只有②③④
A
近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和不锈钢为电极,以KI溶液(加少量K2CrO4)为电解液在一定条件下电解,反应方程式为KI+3H2O![]() KIO3+3H2↑。下列有关说法正确的是 ( )
KIO3+3H2↑。下列有关说法正确的是 ( )
A 电解时,石墨作阴极,不锈钢作阳极
B 电解液调节至强酸性比较合适
C 电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
D 电解中每转移0.6mol电子,理论上可得到21.4g无水KIO3晶体
D
将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,称为燃料电池。下列叙述中正确的是
①通人CH4的电极为正极;
②正极的电极反应式为:O2 + 2H2O + 4e ==== 4OH-
③通人CH4的电极反应式为:CH4+ 2O2+ 4e ==== CO2 +2H2O
④负极的电极反应式为:CH4+ 10 OH-- 8e ===== CO32- + 7H2O
⑤放电时溶液中的阳离子向负极移动;
⑥放电时溶液中的阴离于向负极移动。
⑦工作时正极区pH升高,负极区pH降低
A.①③⑤⑦ B.②④⑥⑦ C. ②④⑤⑥ D.①②③④
B
下列四种装置中,溶液的体积均为250毫升,开始时电解质溶液的浓度均为0.10摩/升,工作一段时间后,测得导线上均通过0.02摩电子,若不考虑溶液体积的变化,则下列叙述正确的是 ( )
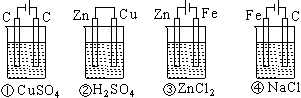
A 工作一段时间后溶液的浓度①=②=③=④
B 工作一段时间后溶液的pH值:④>③>①>②
C 产生气体的总体积:④>③>①>②
D 电极上析出的固体的质量:①>②>③>④
B
本卷还有11题,登录并加入会员即可免费使用哦~

该作品由: 用户魏菲分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。