化学与人类的生产、生活、科技、航天等方面密切相关。下列说法正确的是
A. 汝窑瓷器的天青色来自氧化铁
B. “傍檐红女绩丝麻”所描述的丝、麻主要成分是蛋白质
C. 中国歼—20上用到的氮化镓材料是作为金属合金材料使用
D. 诗句“煮豆燃豆萁”中涉及的能量变化主要是化学能转化为热能和光能
【答案】D
【解析】
【详解】A.氧化铁是红棕色的,所以汝窑瓷器的天青色来自氧化铁说法是错误的,故A错误;
B.丝指蛋白质,麻指纤维素,故B错误;
C.氮化镓是化合物,不属于合金,故C错误;
D.煮豆燃豆萁,豆萁燃烧发光放热,由化学能转化为热能和光能,故D选项正确;
所以本题答案:D。
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1LpH=6的纯水中含有OH-的数目为10-8NA
B. 当氢氧酸性燃料电池中转移2mol电子时被氧化的分子数为NA
C. 0.5mol雄黄(As4S4,结构如图![]() ),含有NA个S—S键
),含有NA个S—S键
D. 一定条件下向密闭容器中充入1molH2和2molH2(g)充分反应,生成HI分子数最多等于2NA
【答案】B
【解析】
【详解】A.纯水中氢离子和氢氧根离子浓度相等,所以pH=6的纯水中,氢氧根离子浓度为l×10-6mol/L,1L纯水中含有的OH-数目为l×10-6NA,故A错误;
B. 氢氧燃料电池在酸性条件下,负极的电极反应式为:H2-2e-=2H+,正极的电极反应式为:4H++O2+4e-=2H2O,当转移2mol电子时,被氧化的分子数为NA,故B正确;
C. 由雄黄的结构简式:![]() 可知,结构中不存在S—S ,所以C错误;
可知,结构中不存在S—S ,所以C错误;
D. 因为H2+I2![]() 2HI为可逆反应,所以一定条件下向密闭容器中充入1molH2和2molI2(g)充分反应,生成HI分子数小于2NA,故D错误;
2HI为可逆反应,所以一定条件下向密闭容器中充入1molH2和2molI2(g)充分反应,生成HI分子数小于2NA,故D错误;
所以本题答案:B。
某课外小组在实验室模拟工业上从浓缩海水中提取溴的工艺流程,设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。下列说法错误的是
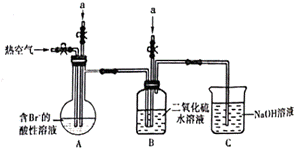
A. 装置中通入的是a气体是Cl2
B. 实验时应在A装置中通入a气体一段时间后,停止通入,改通入热空气
C. B装置中通入a气体前发生的反应为SO2+ Br2+2H2O===H2SO4+2HBr
D. C装置的作用只是吸收多余的二氧化硫气体
【答案】D
【解析】
【分析】
实验室模拟工业上从浓缩海水中提取溴,由实验装置可知,a中气体为氯气,在A中氯气可氧化溴离子,利用热空气将溴单质吹出,B中通入气体为二氧化硫,在B中发生SO2+Br2+2H2O=H2SO4+2HBr,c中NaOH溶液可吸收溴、氯气、二氧化硫等尾气,以此来解答。
【详解】A.A装置中通入的a气体是Cl2,目的是氧化A中溴离子,故A正确;
B.实验时应在A装置中通入a气体一段时间后,停止通入,改通入热空气,热空气将溴单质吹出,故B正确;
C.B装置中通入b气体后发生的反应为SO2+Br2+2H2O=H2SO4+2HBr,故C正确;
D.C装置![]() 作用为吸收溴蒸汽、氯气、二氧化硫等尾气,故D错误;
作用为吸收溴蒸汽、氯气、二氧化硫等尾气,故D错误;
所以本题答案:D。
【点睛】解题依据物质氧化性强弱。根据Cl2氧化性大于Br2,可以把Br-氧化成溴单质,结合实验原理选择尾气处理试剂。
由C、H、O中两种或三种元素组成的儿种有机物模型如下,下列说法正确的是
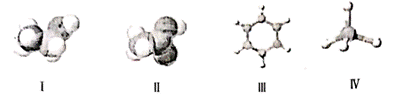
A. 上述四种有机物均易溶于水 B. 有机物Ⅳ的二氯代物有2种
C. 一定条件下有机物III能与氢气发生加成 D. I生成Ⅱ的反应类型为还原反应
【答案】C
【解析】
【详解】A.苯和甲烷都不溶于水,故上述四种有机物均易溶于水说法是错误的,故A错误;
B.IV为甲烷,属于正四面体结构,所以其二氯代物有1种,故B错误;
C.III是苯,结构简式为:![]() ,一定条件下能与氢气发生加成,故C正确;
,一定条件下能与氢气发生加成,故C正确;
D.I为乙醇,结构简式为:CH3CH2OH;II为乙酸,结构简式为:CH3COOH,I生成Ⅱ的反应类型为氧化反应,故D错误;
所以本题答案:C。
【点睛】由几种有机物模型分析:I为乙醇,结构简式为:CH3CH2OH;II为乙酸,结构简式为:CH3COOH;III苯,结构简式为:![]() ;IV为甲烷,结构简式为:CH4,结合几种物质的性质回答。
;IV为甲烷,结构简式为:CH4,结合几种物质的性质回答。
下列实验操作和现象对应的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将铜片和铁片用导线连接插入浓硝酸中,铁片表面产生气泡 | 金属铁比铜活泼 |
| B | 常温下,测定同浓度NaA和NaB溶液的pH:NaA小于NaB | 相同条件下,在水中HA电离程度大于HB |
| C | 加热含有酚酞的Na2CO3溶液,溶液红色加深 | CO32-的水解反应是吸热反应 |
| D | 向饱和FeSO4溶液中加入CuS固体,测得溶液中c(Fe2+)不变 | Ksp(CuS)<Ksp (FeS) |
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.将铜片和铁片导线连接插入浓硝酸中,由于铁与浓硝酸发生钝化反应,所以铁为正极,铜为负极,但金属活动性Fe大于Cu,故A错误。
B. 常温下,测定同浓度NaA和NaB溶液的pH:NaA小于NaB,说明HA的酸性比HB强,相同条件下,在水中HA电离程度大于HB,故B正确;
C. 加热促进盐类水解,Na2CO3溶液水解显碱性,加热含有酚酞的Na2CO3溶液,溶液红色加深,所以CO32-的水解反应是吸热反应,故C正确;
D. 向饱和FeSO4溶液中加入CuS固体,测得溶液中c(Fe2+)不变,说明没有FeS 生成,所以说明Ksp(CuS)<Ksp (FeS),故D正确;
所以本题答案:A。
【点睛】注意点:铁与浓硝酸发生钝化反应,生成的氧化膜组织铁继续被氧化。所以铜和铁做电极材料的时候,铜先放电做原电池的负极。
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户毛嘉青分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。