在一密闭容器中盛有V LCl2和H2的混合气体,用电火花引燃后,恢复到原来状态,发现混合气体仍为V L,用足量的NaOH溶液吸收引燃后的混合气体,结果无气体剩余。由以上知,原混合气体中Cl2和H2的体积比一定为
A.小于1 B.小于等于1 C.等于1 D.大于等于1
D
下列反应离子方程式中不正确的是
A.向澄清石灰水中通入过量的二氧化碳: CO2+OH=HCO3-
B.向漂白粉溶液中通过量的二氧化碳: CO2+OH=HCO3-
C.向漂白粉溶液中通入过量的二氧化硫:SO2+OH-=HSO3-
D.向硫酸氢钠溶液中加入过量的氢氧化钡:Ba2++2OH-+2H++SO42=BaSO4↓+2H2O
BC
右图中A处通入Cl2,关闭B阀时,C处红色布条无变化;打开B阀时,C处红色布条褪色,则D中的溶液是
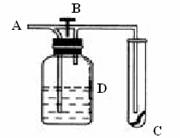
A.浓H2SO4 B.H2O
C.饱和NaOH溶液 D.饱和食盐水
AC
某化学兴趣小组设计用实验室里的常规仪器制取少量漂白粉。可以选用的仪器有A~H,其中分液漏斗里均盛有浓盐酸,A的大试管里及烧瓶中均装有一定量的二氧化锰固体,B和H的U形管内均装有消石灰,B的水槽里盛有冰水,D中装有澄清石灰水,E中装有浓氢氧化钠溶液。已知,氯气与氢氧化钙的反应是放热的,而在温度稍高时氯气与氢氧化钙就会发生副反应而生成氯酸钙等副产物。
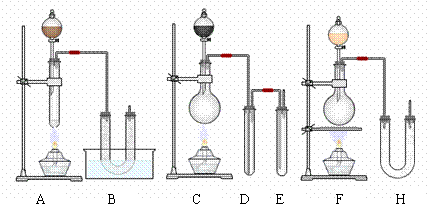
(1)请你根据实际需要,从A~H中选出最合理的仪器组装成一套制取少量漂白粉的实验装置(用序号表示,并要按照最合理的顺序从左到右排列) 。
(2)若由AB组成的装置是甲同学设计的,由CDE组合成的装置是乙同学设计的,由FH组合成的装置是丙同学设计的,请你分析甲、乙、丙三套装置的优缺点。
| 装置序号 | 优点 | 缺点 |
| 甲 | ||
| 乙 | ||
| 丙 |
(1)FBE(2)
| 装置序号 | 优点 | 缺点 |
| 甲 | 有冷凝装置,可避免副反应发生 | 不能控制盐酸的加入量,不容易控制反应速率;无尾气处理装置,易产生污染 |
| 乙 | 有尾气处理装置,能防止污染坏境 | 不能控制盐酸的加入量,不容易控制反应速率;无冷凝装置,不能避免副反应发生;澄清石灰水浓度小,不适宜于制漂白粉 |
| 丙 | 能控制盐酸的加入量,容易控制反应的速率 | 无冷凝装置,不能避免副反应的发生;无尾气处理装置,易产生污染 |
用滴管将新制的饱和氯水慢慢滴入到含有酚酞的NaOH稀溶液中,当滴到最后一滴时,红色突然褪去,分析产生上述现象的原因,估计可能有两种:一是由于氯水中的HClO强氧化性,把酚酞氧化而漂白退色;二是由 。请你与同学讨论设计一个简单实验证明以上两个推测是否正确。
实验方案: ;
结论: 。
另一个可能是氯水中的盐酸中和了NaOH,而使溶液褪色。
实验方案:向褪色的溶液中再加滴加少量的NaOH溶液。
结论:若变红,则推测正确,若不变红,则是HClO的氧化作用把酚酞氧化而褪色。
本卷还有2题,登录并加入会员即可免费使用哦~

该作品由: 用户莫歌分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。