下列说法正确的是( )
①需要加热方能发生的反应一定是吸热反应
②放热反应在常温下一定很容易发生
③反应是放热还是吸热必须看反应物和![]() 生成物所具有的总能量的相对大小
生成物所具有的总能量的相对大小
④放热反应加热到一定温度引发后,停止加热反应也能继续进行
A.③④ B.①②
C.①②③④ D.②③④
解析:需要加热才能发生的反应不一定是吸热反应,如铝热反应;放热反应常温下不一定容易发生,如铝热反应;反应是放热还是吸热取决于反应物、生成物所具有的总能量的相对大小;由于放热反应在反应过程中放出热量,可以维持反应的继续进行,所以停止加热后反应也可以继续进行。
答案:A
下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与CO2的反应
D.甲烷在氧气中的燃烧
解析:2Al+6HCl===2AlCl3+3H2↑既属于氧化还原反应,又属于放热反应,A项错误;Ba(OH)2·8H2O+2NH4Cl===Ba![]() Cl2+2NH3↑+10H2O属于非氧化还原反应,但属于吸热反应,B项错误;灼热的碳与CO2的反应既是氧化还原反应又是吸热反应,C项正确;甲烷在氧气中燃烧是氧化还原反应,也是放热反应,D项错误。
Cl2+2NH3↑+10H2O属于非氧化还原反应,但属于吸热反应,B项错误;灼热的碳与CO2的反应既是氧化还原反应又是吸热反应,C项正确;甲烷在氧气中燃烧是氧化还原反应,也是放热反应,D项错误。
答案:C
.已知2SO2+O2![]() 2SO3为放热反应,对该反应的下列说法正确的是( )
2SO3为放热反应,对该反应的下列说法正确的是( )
A.O2的能量一定高于SO2的能量
B.SO2和O2的总能量一定高于SO3的总能量
C.SO2的能量一定高于SO3的能量
D.因该反应为放热反应,故不必加热就可发生
解析:判断一个反应是放热反应还是吸热反应,关键看反应物的总能量与生成物的总能量的差值。如果反应物的总能量高于生成物的总能量,反应放热,B项正确;A项和C项错误,都没有考虑总能量差;放热反应只表明反应物总能量比生成物总能量高,而加热是反应的条件,两者无必然联系,许多放热反应也必须加热才![]() 能开始进行,D项错误。
能开始进行,D项错误。
答案:B
化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
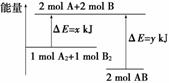
A.该反应是吸热反应
B.1 mol A—A键和1 mol B—B键断裂能放出x kJ的能量
C.2 mol A—B键断裂需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
解析:由图知1 mol A2和1 mol B2的总能量大于2 mol AB的总能量,该反应为放热反应,A、D错误;化学键断裂时吸热,B错误;由图知2 mol A—B键断裂吸收y kJ的能量,C正确。
答案:C
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,断裂1 mol H2中的化学键消耗的能量为Q1 kJ,断裂1 mol Cl2中的化学键消耗的能量为Q2 kJ,形成1 mol HCl中的化学键释放的能量为Q3 kJ。下列关系式中,正确的是( )
A.Q1+Q2>Q3 B.Q1+Q2>2Q3
C.Q1+Q2<Q3 D.Q1+Q2<2Q3
解析:H2在Cl2中燃烧为放热反应,故断裂化学键消耗的能量总和(Q1+Q2)小于形成化学键释放的能量总和(2Q3)。即Q1+Q2<2Q3。
答案:D
本卷还有10题,登录并加入会员即可免费使用哦~

该作品由: 用户王俊仁分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。