下面有关Na2CO3 与NaHCO3的叙述错误的是 ( )![]()
A. Na2CO3遇少量酸可转化为NaHCO3
B. 在水中的溶解度Na2CO3比NaHCO3大
C. 与同浓度的硫酸反应时,Na2CO3比NaHCO3剧烈
D. NaHCO3能与NaOH反应,而Na2CO3不能
【答案】C

下列实验过程中产生的现象与对应的图象不相符的是( )
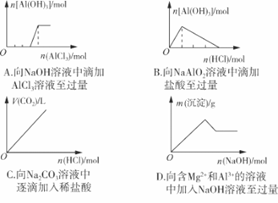
【答案】C
【解析】A.NaOH溶液和AlCl3溶液按4∶1混合后完全转化为NaAlO2,继续加入AlCl3溶液,发生反应为Al3++3AlO2-+6H2O===4Al(OH)3↓,故A与图相符;B.NaAlO2溶液中加入盐酸立即有沉淀生成,继续加入盐酸,沉淀溶解,其反应为NaAlO2+HCl+H2O===Al(OH)3↓+NaCl,Al(OH)3+3HCl===AlCl3+3H2O,B与图相符;C.Na2CO3溶液中加入盐酸先转化为NaHCO3和NaCl,Na2CO3完全转化为NaHCO3后,再加入盐酸才产生气体,C与图不相符;D.向含Mg2+和Al3+的溶液中加入NaOH溶液得到Mg(OH)2和Al(OH)3两种沉淀,继续加入NaOH溶液,Al(OH)3沉淀溶解,D与图相符。
向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入 一定量的CO2得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1 mol·L-1盐 酸。此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所 示。则下列叙述中正确的是
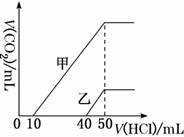
A. 原NaOH溶液的物质的量浓度为0.5 mol·L-1
B. 当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为 OH-+H+=H2O
C. 乙溶液中含有的溶质是Na2CO3、NaHCO3
D. 乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况)
【答案】A
将NaAlO 2、Ba(OH) 2、NaOH配成100.0 mL混合溶液,向该溶液中通入足量CO 2,生成沉淀的物质的量n(沉淀),与通入CO 2的物质的量n(CO 2)的关系,如图所示, 下列说法中正确的是
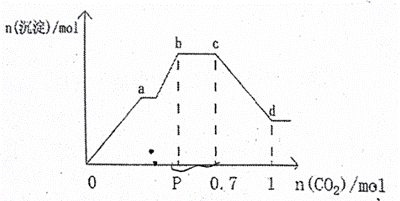
A. P点的值为0.6
B. 混合溶液中c(NaOH)+c(NaAlO2)=4.0 mol/L
C. bc段的化学反应方程式为:NaOH+CO2=NaHCO3
D. cd段表示Al(OH)3沉淀溶解
【答案】B
【解析】A. 根据上述分析,b点对应的溶液中含有碳酸钠,c点对应的溶液中含有碳酸氢钠,d点对应的溶液中含有碳酸氢钠和碳酸氢钡,溶解碳酸钡消耗的二氧化碳为1mol-0.7mol=0.3mol,因此原混合溶液中含有0.3mol Ba(OH)2;c点对应的溶液中含有碳酸氢钠,根据碳元素守恒,生成碳酸氢钠和碳酸钡共消耗0.7mol二氧化碳,因此碳酸氢钠的物质的量为0.7mol -0.3mol=0.4mol,根据钠元素守恒,混合溶液中n(NaOH)+n(NaAlO2) =0.4 mol,b点消耗的二氧化碳是与NaAlO2、Ba(OH)2、NaOH反应生成碳酸钡,氢氧化铝和碳酸钠的二氧化碳的总量,根据CO2+Ba(OH)2═BaCO3↓+H2O、CO2+2NaOH═Na2CO3+H2O、CO2+3H2O+2NaAlO2═2Al(OH)3↓+Na2CO3可知,n (CO2)=n[Ba(OH)2]+ ![]() n(NaOH)+
n(NaOH)+![]() n(NaAlO2)
n(NaAlO2)
=0.3mol+0.2mol=0.5mol,则有P=0.6,故A错误;B. c点对应的溶液中含有碳酸氢钠,根据碳元素守恒,生成碳酸氢钠和碳酸钡共消耗0.7mol二氧化碳,因此碳酸氢钠的物质的量为0.7mol -0.3mol=0.4mol,根据钠元素守恒,混合溶液中c(NaOH)+c(NaAlO2)=![]() =4.0 mol/L,故B正确;C. bc段是碳酸钠溶解的过程,反应的化学反应方程式为:Na2CO3+H2O +CO2=2NaHCO3,故C错误;D. cd段是溶解碳酸钡的过程,故D错误。
=4.0 mol/L,故B正确;C. bc段是碳酸钠溶解的过程,反应的化学反应方程式为:Na2CO3+H2O +CO2=2NaHCO3,故C错误;D. cd段是溶解碳酸钡的过程,故D错误。
本卷还有27题,登录并加入会员即可免费使用哦~

该作品由: 用户angle分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。
