中华传统文化源远流长,古代化学与生产生活密切相关。下列对描述内容分析错误的是
| 选项 | 描述 | 分析 |
| A | “丹砂(HgS)烧之成水银 ,积变又还成丹砂” | 此过程涉及化学变化 |
| B | “用浓酒和糟入甑,蒸令气上……其清如水” | 涉及的操作是蒸馏 |
| C | “以火烧之,紫青烟起,乃真硝石也” | 硝石中含碘单质 |
| D | “采蒿蓼之属,晒干烧灰,以水淋汁,浣衣发面,去垢” | 利用其水解显碱性去污 |
C
为了缓解温空效应,科学家提出了多种回收和利用CO2的方案。
(1) 方案1: 利用FeO吸收CO2获得H2
ⅰ.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ΔH1=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH2 = + 113. 4kJ/mol
则 3FeO(g)+H2O(g)= Fe3O4(s)+H2(g) ΔH3 = 。
方案2:利用CO2制备CH4
 300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应:CO2(g)+4H2(g)
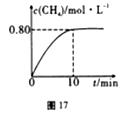
300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应:CO2(g)+4H2(g)![]() CH4(g)+ 2H2O(g)ΔH4,混合气体中CH4的浓度与反应时间的关系如图17所示。
CH4(g)+ 2H2O(g)ΔH4,混合气体中CH4的浓度与反应时间的关系如图17所示。
(2)①从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)= 。
②300℃时,反应的平衡常数K= 。
③保持温度不变,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度 (填序号)。
A.等于0.8mo/L B.等于1.6mo/L C.0.8mol/L<c(CH4)<1.6mol/L D.大于1.6mol/L
(3)300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g).则v正 v逆
(填“>”“<”或“=" )。
(4)已知:200℃时,该反应的平衡常数K=64.8L2·mol-2。则ΔH4 0(填“>”“<”或“=”)。
 方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2
方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图18所示:(假设开始时两极的质量相等)
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图18所示:(假设开始时两极的质量相等)
(5)①放电时,正极的电极反应式为 。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mole-时,两极的质量差为 g。
(6)室温下,物质的量浓度均为0.lmol/L 的几种含碳盐溶液的pH如下表:
| 序号 | ① | ② | ③ |
| 溶液 | NaHCO3 | NaX | Na2CO3 |
| pH | 8.4 | 9.7 | 11.6 |
写出溶液②中通入少量CO2的离子方程式: .
等体积的①和③形成的混合溶液中离子浓度由大到小排列为: .
【答案】(共15分)(1)+18.7kJ/mol (2分)
(2)①0.32mol·L−1·min−1 (1分) ②25 L2·mol−2 (1分) ③D (1分)
(3)> (1分)
(4)< (1分)
(5)①3CO2+4Na++4e−=2Na2CO3+C (2分) ②15.8 (2分)
(6)X−+CO2+H2O=HCO![]() +HX(2分) c(Na+)>c(HCO3-)>c(CO32-)> c(OH-)> c(H+)(2分)
+HX(2分) c(Na+)>c(HCO3-)>c(CO32-)> c(OH-)> c(H+)(2分)
氮及其化合物广泛存在于自然界中。回答下列问题:
(1)写出N原子的电子排布式__________。在基态14N原子中,核外存在______个未成对电子。
(2)原子第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为_______________。
(3)氮气和氢气在一定条件下可合成氨,其中N2中共价键的类型有___________,其个数比为____________;NH3中氮原子的杂化方式为_________杂化。
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因是______________。
(5)X的+1价阳离子中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是_____________,X离子与N3-形成的化合物化学式为________。
 (6)与NO2-等电子体的粒子为:_____________(写出一种即可)。
(6)与NO2-等电子体的粒子为:_____________(写出一种即可)。
【答案】(1)1s22s22p3 (1分) 3(2分)
(2)N>P>As(2 分)
(3)σ键与π键(1分) 1∶2 (1分) sp3 (1分)
(4)HN3分子间存在氢键(2分)
(5)Cu(1分) Cu3N(2分) O3、SO2 、SeO2 (任选一种)(2分)
设NA为阿伏伽德罗常数的值。下列叙述正确的是
A. 1mol甲![]() 醇中含有C—H键的数目为4NA
醇中含有C—H键的数目为4NA
B. 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C. 标准状况下,2.24L已烷含有分子的数目为0.1NA
D. 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转![]() 移电子的数目为0.4NA
移电子的数目为0.4NA
D
下列装置图能达到相应目的的是
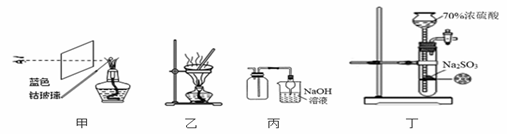
A. 装置甲:检验碳酸钾中钾元素的存在
B. 装置乙:蒸干MgCl2饱和溶液制备MgCl2·6H2O晶体
C. 装置丙:收集NO2并防止其污染环境
D. 装置丁:制备少量SO2
A
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户墨瞳分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。