2017人教版高中化学期末考试129213
高中
整体难度:中等
2017-11-25
题号
一
二
三
四
五
评分
一、选择题 (共16题)
添加该题型下试题
1.
锌粉与碘粉均匀混合,无明显现象,滴加几滴水,发生剧烈反应,并产生大量紫色蒸气,以下叙述错误的是
A. H20作催化剂 B.紫色蒸气是I2
C.该反应是放热反应 D.反应后物质的总能量升高
难度:
知识点:化学反应中的能量变化
使用次数:148
【答案】
D
2.
右图是关于反应(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
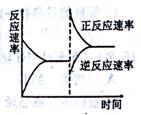 A.升高温度,同时加压
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用正催化剂
难度:
知识点:化学反应速率
使用次数:100
【答案】
C
3.
下列关于电解质溶液的判断正确的是
A.60℃时,NaCl溶液的pH<7,则溶液呈酸性
B.将pH=4的 CH3COOH溶液加水稀释,溶液中所有离子的浓度均减小
C.常温下,CH3COOH分子可能存在于pH>7的减性溶液中
D.相同温度下,1 mol/L氨水与0.5 mol/L氨水中c(OH-)之比是2:1
难度:
知识点:电离平衡单元测试
使用次数:107
【答案】
C
4.
盐MN溶于水存在如图过程,下列有关说法中不正确的是
 A.该过程可表示MN的水解过程
A.该过程可表示MN的水解过程
B.相同条件下结合H+的能力N->OH-
C.该过程使溶液中的c(OH-)>c(H+)]
D. 溶液中存在c(HN)=c(OH-)-c(H+)
难度:
知识点:盐类的水解
使用次数:162
【答案】
B
5.
恒温、恒压下,1 mol A和1 mol B在一个容积可变的容器中发生如下反应:A(g) + 2B(g)= 2C(g)。一段时间后达到平衡,生成a mol C。则下列说法不正确的是
A.物质A、B的转化率之比一定是1:2
B.起始时刻和达平衡后容器中的压强比为1:1
C.若起始放入3 mol A和3 mol U,则达平衡时生成3a mol C
D.当![]() (A)=
(A)= ![]() (B)时,可断定反应达到平衡
(B)时,可断定反应达到平衡
难度:
知识点:化学平衡
使用次数:116
【答案】
D
本卷还有18题,登录并加入会员即可免费使用哦~
立即下载
全选试题
编辑试卷
收藏试卷

试题总数:
23
总体难度:
中等
难度统计
难度系数
数量
占比
容易
7
30.43%
中等
16
69.56%
题型统计
大题类型
数量
占比
选择题
16
69.56%
实验,探究题
1
4.34%
填空题
2
8.69%
综合题
2
8.69%
推断题
2
8.69%
知识点统计
知识点
数量
占比
化学反应中的能量变化
1
4.34%
化学反应速率
1
4.34%
电离平衡单元测试
5
21.73%
盐类的水解
1
4.34%
化学平衡
1
4.34%
电化学 胶体
2
8.69%
原子结构
3
13.04%
物质结构 元素周期律单元测试
6
26.08%
化学键
1
4.34%
烃的衍生物单元测试
2
8.69%
版权提示
该作品由: 用户安雨航分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。