纯碱被视作“碱”用于油污清洗,溶液碱性较强.下列有关分析不正确的是( )
A.纯碱主要成分为Na2CO3 B.热的纯碱溶液去污效果更好
C.纯碱有利于油污水解 D.纯碱常用于治疗胃酸过多
【考点】DD:盐类水解的应用.
【分析】A.纯碱为碳酸钠的俗称;
B.碳酸钠溶液中碳酸根离子水解溶液显碱性,水解过程为吸热反应,升温促进水解正向进行;
C.油污是高级脂肪酸甘油酯,碱性溶液中水解生成易溶于水的物质,便于洗涤;
D.纯碱碱性太强,应用碳酸氢钠;
【解答】解:A.纯碱是碳酸钠的俗称主要成分为Na2CO3,故A正确;
B.碳酸钠溶液中碳酸根离子水解溶液显碱性,CO32﹣+H2O⇌HCO3﹣+OH﹣,水解过程为吸热反应,升温促进水解正向进行,溶液碱性增强热的纯碱溶液去污效果更好,故B正确;
C.油污是高级脂肪酸甘油酯,碱性溶液中水解生成易溶于水的物质,便于洗涤,纯碱有利于油污水解,故C正确;
D.纯碱碱性较强,腐蚀性强,若遇到胃溃疡会造成胃穿孔,故D错误;
故选D.
由分类思想,下列说法正确的是( )
A.氢氧化钠溶液、盐酸都为强电解质
B.铁生锈、食物腐败都涉及有氧化还原反应
C.漂白粉、冰醋酸、氢氧化铁胶体均为混合物
D.二氧化氮、二氧化硅都是酸性氧化物
【考点】3A:酸、碱、盐、氧化物的概念及其相互联系;37:混合物和纯净物;B1:氧化还原反应;D2:强电解质和弱电解质的概念.
【分析】A.水溶液中或熔融状态下完全电离的电解质为强电解质;
B.铁生锈与食物腐败均属于缓慢氧化;
C.不同物质组成的为混合物;
D.酸性氧化物是与碱反应只生成盐和水的氧化物.
【解答】解:A.盐酸属于混合物,既不是电解质也不是非电解质,故A错误;
B.食物腐败与铁生锈均属于缓慢氧化,都涉及有氧化还原反应,故B正确;
C.漂白粉是氯化钙和次氯酸钙的混合物、冰醋酸是一种物质组成的纯净物、氢氧化铁胶体为混合物,故C错误;
D.二氧化硅和碱反应生成盐和水属于酸性氧化物,二氧化氮和碱反应发生氧化还原反应,不是酸性氧化物,故D错误;
故选B.
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.2 mol Na2O2和Na2S的混合物中共含有离子数目为0.6 NA
B.1 mol Cl2溶于水的过程中有NA个电子转移
C.常温下,pH=12的氢氧化钠溶液中OH﹣数目为0.01 NA
D.1.0 mol/L FeCl3溶液全部转化成氢氧化铁胶体所得胶粒数目为NA
【考点】4F:阿伏加德罗常数.
【分析】A、Na2O2和Na2S均由2个阳离子和1个阴离子构成;
B、氯气和水的反应为可逆反应;
C、溶液体积不明确;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,且氯化铁溶液体积不明确.
【解答】解:A、Na2O2和Na2S均由2个阳离子和1个阴离子构成,故0.2mol过氧化钠和硫化钠的混合物中含0.6NA个离子,故A正确;
B、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子数小于NA个,故B错误;
C、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故C错误;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,且氯化铁溶液体积不明确,故形成的胶粒的个数无法计算,故D错误.
故选A.
下列操作或装置能达到实验目的是( )
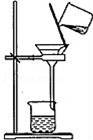
| 选项 | A | B | C | D |
| 操作或装置 |
|
|
|
|
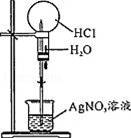
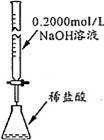
| 目的 | 配制一定物质的量浓度溶液 | 分离Na2CO2溶液和CH3COOC2H5的混合物 | 做“白色”喷泉实验 | 用NaOH溶液滴定稀盐酸 |
A.A B.B C.C D.D
【考点】U5:化学实验方案的评价;QB:实验装置综合.
【分析】A.转移液体需要引流;
B.Na2CO2溶液和CH3COOC2H5的混合物分层;
C.HCl与硝酸银溶液反应生成白色沉淀,烧瓶内气体减少,外压大于内压;
D.NaOH不能用酸式滴定管盛放.
【解答】解:A.转移液体需要引流,图中缺少玻璃棒,故A错误;
B.Na2CO2溶液和CH3COOC2H5的混合物分层,应选分液装置,而图中为过滤装置,故B错误;
C.HCl与硝酸银溶液反应生成白色沉淀,烧瓶内气体减少,外压大于内压,则图中装置可做白色”喷泉实验,故C正确;
D.NaOH不能用酸式滴定管盛放,应选碱式滴定管,故D错误;
故选C.
下列离子方程式正确的是( )
A.向硫酸铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2﹣+4NH4++2H2O
B.少量双氧水滴入酸性KI溶液:2H2O2+2I﹣+4H+═4H2O+I2
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O
D.碱性锌锰电池正极反应:2MnO2+2H2O+2e﹣═2MnOOH+2OH﹣
【考点】49:离子方程式的书写.
【分析】A.氢氧化铝不溶于弱碱氨水;
B.二者反应生成碘和水,转移电子不守恒;
C.二者反应生成硝酸铁、NO和水,磁性氧化铁为四氧化三铁,应该写化学式;
D.正极上二氧化锰得电子生成MnOOH和OH﹣.
【解答】解:A.氢氧化铝不溶于弱碱氨水,离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A错误;
B.二者反应生成碘和水,转移电子不守恒,离子方程式为H2O2+2I﹣+2H+═2H2O+I2,故B错误;
C.二者反应生成硝酸铁、NO和水,磁性氧化铁为四氧化三铁,应该写化学式,离子方程式为3Fe3O4+NO3﹣+28H+═9Fe3++14H2O+NO↑,故C错误;
D.正极上二氧化锰得电子生成MnOOH和OH﹣,离子方程式为2MnO2+2H2O+2e﹣═2MnOOH+2 OH﹣,故D正确;
故选D.
本卷还有9题,登录并加入会员即可免费使用哦~

该作品由: 用户小小分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。