用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,2.24L甲烷、戊烷混合物所含分子数为0.1NA
B. 0.1molC2H6O分子中含有的C-H的数目一定为0.5NA
C. 1L lmol/L的CH3COONa溶液中所含CH3COO-个数为NA
D. 标准状况下,2.24L16O2和3.6g18O2含有氧原子均为0.2NA
D
【解析】A. 标准状况下,戊烷不是气体,2.24L甲烷、戊烷混合物所含分子数多于0.1NA,故A错误;B. C2H6O可能是乙醇也可能是二甲醚,0.1molC2H6O分子中含有的C-H的数目可能为0.5NA或0.6NA,故B错误;C. 醋酸钠溶液中醋![]() 酸根离子要水解,1L lmol/L的CH3COONa溶液中所含CH3COO-个数少于NA,故C错误;D. 标准状况下,2.24L16O2的物质的量为0.1mol,3.6g18O2的物质的量为0.1mol,含有氧原子均为0.2NA,故D正确;故选D。
酸根离子要水解,1L lmol/L的CH3COONa溶液中所含CH3COO-个数少于NA,故C错误;D. 标准状况下,2.24L16O2的物质的量为0.1mol,3.6g18O2的物质的量为0.1mol,含有氧原子均为0.2NA,故D正确;故选D。
下列的实验操作中所用仪器合理的是 ( )
A. 用25 mL的酸式滴定管量取14.80 mL 高锰酸钾溶液
B. 用100 mL量筒量取5.2 mL盐酸
C. 用托盘天平称取25.20 g氯化钠
D. 用100 mL![]() 容量瓶配制50 mL 0.1 mol / L盐酸
容量瓶配制50 mL 0.1 mol / L盐酸
A
在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是 ( )
A. 气体A与气体B的相对分子质量比为m:n
B. 同质量的气体A与B的分子个数比为n:m
C. 同温同压下,A气体与B气体的密度比为n:m
D. 同温同压下,同体积的A气体与B气体的质量比为m:n
C
【解析】标准状况下,分子数相同的气体A和B,它们的物质的量相同,气体体积相同.
A.M=![]() 可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确;B.A与B相对分子质量之比为m:n,同质量时由n=
可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确;B.A与B相对分子质量之比为m:n,同质量时由n=![]() 可知,分子数之比等于
可知,分子数之比等于![]() ∶
∶![]() =n∶m,故B正确;C.同温同压,气体密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故C错误;D.相同状况下,同体积的A与B的物质的量相同,则质量之比等于相对分子质量之比,即为m:n,故D正确;故选C。
=n∶m,故B正确;C.同温同压,气体密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故C错误;D.相同状况下,同体积的A与B的物质的量相同,则质量之比等于相对分子质量之比,即为m:n,故D正确;故选C。
把VL含MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1
mol·L-1
C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
D
【解析】混合溶液分成两等份,每份溶液浓度与原溶液浓度相同,一份加BaCl2的溶液发生Ba2++SO42-═BaSO4↓,由方程式可知n(SO42-)=n(Ba2+)=n(BaCl2)=bmol,另一份加氢氧化钠溶液时发生Mg2++2OH-═Mg(OH)2 ↓,由方程式可知每份溶液中n(Mg2+)=1/2n(OH-)=1/2amol,由电荷守恒可知每份中2n(Mg2+)+n(K+)=2n(SO42-),故每份中溶液n(K+)=2b-2×1/2amol=(2b-a)mol,则原混合溶液中钾离子的浓度为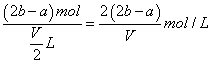 ,故选D.
,故选D.
某结晶水合物的化学式为R•nH2O,其相对分子量为M。25℃时,将ag该晶体溶于bg水中恰好形成VmL饱和溶液,下列关系式正确的是( )
A. 饱和溶液的物质的量浓度为c=![]() mol·L-1
mol·L-1
B. 饱和溶液中溶质的质量分数为w=![]() %
%
C. 25℃时R的溶解度为S=![]() g
g
D. 饱和溶液的密度为ρ=![]() g·L-1
g·L-1
C
【解析】A、溶质的物质的量为n=a/M,溶液的物质的量浓度= a/M /(V×10-3)=1000a/MVmol/L,A错误;B、溶质的质量= ![]() ,所以饱和溶液的质量分数=
,所以饱和溶液的质量分数= 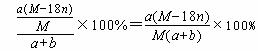 ,B错误;C、溶质的质量为
,B错误;C、溶质的质量为![]() ,溶剂的质量为18na/M+b,所以其溶解度=100×
,溶剂的质量为18na/M+b,所以其溶解度=100×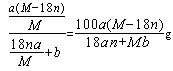 ,C正确; D、溶液的质量为a+b,溶液的密度=质量/体积=(a+b)/V,D错误,答案选C。
,C正确; D、溶液的质量为a+b,溶液的密度=质量/体积=(a+b)/V,D错误,答案选C。
本卷还有17题,登录并加入会员即可免费使用哦~

该作品由: 用户周淑娟分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。