参考下表键能数据,估算晶体硅在氧气中燃烧生成的二氧化硅晶体的热化学方程式:
Si(s)+O2(g)===SiO2(s)中,ΔH的值为( )
| 化学键 | Si—O | O===O | Si—Si | Si—Cl | Si—C |
| 键能/ | |||||
| kJ·mol-1 | 460 | 498.8 | 176 | 360 | 347 |
A.-989.2 kJ·mol-1 B.+989.2 kJ·mol-1
C.-61.2 kJ·mol-1 D.-245.2kJ·mol-1
答案 A
解析 硅和二氧化硅均是原子晶体,其中在晶体硅中每个硅原子形成2个Si—Si键,在二氧化硅晶体中每个硅原子形成4个Si—O键。由于反应热等于断键吸收的能量与形成化学键所放出的能量的差值,则该反应的反应热ΔH=2×176 kJ·mol-1+498.8 kJ·mol-1- 4×460 kJ·mol-1=-989.2 kJ·mol-1,答案选A。
燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图。下列说法正确的是( )

A.镁作Y电极
B.电池工作时Na+向负极移动
C.废液的pH大于NaClO溶液的pH
D.X电极上发生的反应:ClO-+2H2O-4e-===ClO![]() +4H+
+4H+
答案 A
解析 根据OH-移向,X为正极,Y为负极,其电极反应式分别为X:ClO-+2e-+H2O===
Cl-+2OH-;Y:Mg-2e-+2OH-===Mg(OH)2。C项,废液为NaCl,所以废液的pH应小于NaClO溶液的pH。
某电化学气敏传感器的工作原理如图所示,下列说法正确的是( )
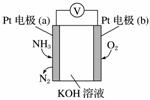
A. b极为负极
B.a极的电极反应式为2NH3+3O2--6e-===N2+3H2O
C.反应消耗的NH3与O2的物质的量之比为4∶5
D.该传感器在工作过程中KOH的物质的量不变
答案 D
解析 根据a,b两极参与反应的物质可以判断a为负极,b为正极,其电极反应式分别:a(负极)2NH3-6e-+6OH-===N2↑+6H2O,
b(正极)![]() O2+6e-+3H2O===6OH-
O2+6e-+3H2O===6OH-
C项,反应消耗NH3与O2的物质的量之比为2∶![]() =4∶3。
=4∶3。
一种碳纳米管能够吸附氢气,可做二次电池(如图所示)的碳电极。该电池的电解质为6
mol·L-1KOH溶液,下列说法中正确的是( )
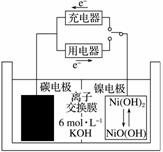
A.充电时阴极发生氧化反应
B.充电时将镍电极与电源的负极相连
C.放电时碳电极反应为H2-2e-===2H+
D.放电时镍电极反应为NiO(OH)+H2O+e-===Ni(OH)2+OH-
答案 D
解析 A项,充电时阴极应发生还原反应,错误;B项,根据放电时电子移向,镍电极为正极,所以充电时应与电源的正极相连;C项,由于电解质溶液为KOH溶液,所以放电时,碳电极反应为H2-2e-+2OH-===2H2O。
下图是一种蓄电池的示意图。被膜隔开的电解质分别为Na2S2和NaBr3,放电后变为Na2S4和NaBr。已知放电时Na+ 由乙池向甲池移动。下面对该装置工作过程中叙述正确的是( )
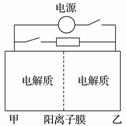
A.放电过程,甲池发生氧化反应
B.放电过程,电池反应:2S![]() + Br
+ Br![]() ===S
===S![]() + 3Br-
+ 3Br-
C.充电过程,乙池为阳极室
D.充电过程,当阴极室阴离子增加2 mol,整个电路中电子转移2 mol
答案 B
解析 根据放电时Na+由乙池向甲池移动,可以判断,乙池为负极室,甲池为正极室,放电时电极反应:负极2S![]() -2e-===S
-2e-===S![]() ,正极:Br
,正极:Br![]() +2e-===3Br-。A项,放电时正极室发生还原反应;C项,充电时,乙池为阴极室;D项,充电时,阴极电极反应为S
+2e-===3Br-。A项,放电时正极室发生还原反应;C项,充电时,乙池为阴极室;D项,充电时,阴极电极反应为S![]() +2e-===2S
+2e-===2S![]() ,当增加2 mol阴离子时,整个电路中应转移4 mol电子。
,当增加2 mol阴离子时,整个电路中应转移4 mol电子。
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户shjsjh分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。