 已知某放热热反应在1L的密闭容器中进行反应。保持容器体积不变,改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各气体物质浓度随时间变化的曲线如下图所示:
已知某放热热反应在1L的密闭容器中进行反应。保持容器体积不变,改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各气体物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)写出该反应的化学方程式 ;
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、
vⅢ(A)从小到大排列次序为 ;
(3)由第二次平衡到第![]() 三次平衡,平衡移动的方向是 (填“正向移动”“逆向移动”“不移动”),改变的条件是 ;
三次平衡,平衡移动的方向是 (填“正向移动”“逆向移动”“不移动”),改变的条件是 ;
(4)在Ⅰ阶段20min时,若在恒温恒压条件下再向该体系中通入3mol A,1mol B,2 molC,则化学平衡 .(填“正向移动”“逆向移动”“不移动”或“无法确定”).
(1)A(g)+3B(g) ![]() 2C(g)
2C(g)
(2)vⅢ(A)<vⅡ(A)<vⅠ(A)
(3)正向移动 降低温度
(4)逆向移动 [解析]因为该温度下化学平衡常数K=![]() 恒压条件下通入3mol A,1mol B,2 molC,体积增大到原来2倍,
恒压条件下通入3mol A,1mol B,2 molC,体积增大到原来2倍,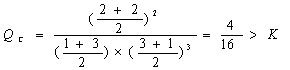 所以平衡逆向移动。
所以平衡逆向移动。
锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为 6C +xLi++xe-===LixC6。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
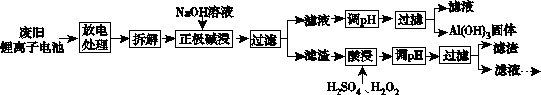

回答下列问题:
(1)Co元素在元素周期表中的位置为 。
(2)“酸浸”一般在80 ℃下进行,写出该步骤中发生的一个主要氧化还原反应的化学方程式__________;可用盐酸代替H2SO4和H2O2的混合液,但缺点是__________________。
(3)写出“沉钴”过程中发生反应的离子方程式_________![]() _____________________。
_____________________。
(4)充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出放电时电池的正极反应方程式_____________________________。
(5)在整个回收工艺中,可回收到的金属化合物有(填化学式)____________。
(1)第四周期Ⅷ族
(2)2LiCoO2+3H2SO4+H2O2Li2SO4+2CoSO4+O2↑+4H2O
有氯气生成,污染较大
(3) Co2++2HCO3—===CoCO3↓+H2O+CO2↑
(4)Li1-xCoO2+xLi++xe-===LiCoO2
(5) Al(OH)3、CoCO3、Li2SO4(错1个 不给分)
碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈、二氧化硅等。水垢会形成安全隐患,需及时清洗除去。清洗流程如下:
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
(1)写出除硫酸钙所涉及的两个化学方程式是 。
(2)在步骤Ⅱ中:
①被除掉的水垢除铁锈外,还有____________________。(填化学式)
②清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因 。
(3)步骤Ⅲ中,加入Na2SO3的目的是________________________________________。
(4)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe2O3保护膜。
①完成并配平其反应的离子方程式:
![]() Fe+
Fe+![]() NO
NO![]() +
+![]() ===
===![]() N2↑+
N2↑+![]() ______+
______+![]() ________
________
②下面检测钝化效果的方法合理的是________。(双选)
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
d.在炉面上滴加浓HNO3,观察出现红棕色气体的时间
(1) CaSO4+Na2CO3===CaC![]() O3+Na2SO4 CaCO3+2HCl===CaCl2+H2O+CO2↑(错1个 不给分)
O3+Na2SO4 CaCO3+2HCl===CaCl2+H2O+CO2↑(错1个 不给分)
(2)① CaCO3、Mg(OH)2、SiO2(错1个 不给分) ②2Fe3++Fe===3Fe2+
(3)将Fe3+还原成Fe2+,防止Fe3+腐蚀锅炉
(4)① 2 2 1H2O 1 1Fe2O3 2OH- (错1个 不给分)
②bc(错1个 不给分)
丙烯腈(CH2===CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产。主要副产物有丙烯醛(CH2===CHCHO)和乙腈(CH3CN)等。回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+![]() O2(g)===C3H3N(g)+3H2O(g) ΔH=-515 kJ·mol-1
O2(g)===C3H3N(g)+3H2O(g) ΔH=-515 kJ·mol-1
②C3H6(g)+O2(g)===C3H4O(g)+H2O(g) ΔH=-353 kJ·mol-1
两个反应在热力学上趋势均很大,其原因![]() 是______________________________;有利于提高丙烯腈平衡产率的反应条件是____________________________。
是______________________________;有利于提高丙烯腈平衡产率的反应条件是____________________________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460 ℃。低于460 ℃时,丙烯腈的产率________(填“是”或“不是”)对应温度下的平衡产率,判断理由是_____.

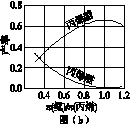
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,进料气氨、丙烯、空气的理论最佳体积比约为_________________。
(1)两个反应均为放热量大的反应(2分) 降低温度降低压强(2分)
(2)不是(1分) 该反应为放热反应,平衡产率应随温度升高而降低 (2分)
(3) 1∶1∶7.5(或2:2:15)(2分)
某含铬Cr2O72- 废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。![]() 该沉淀干燥后得到n molFeO·FeyCrxO3 。不考虑处理过程
该沉淀干燥后得到n molFeO·FeyCrxO3 。不考虑处理过程![]() 中的实际损耗,下列叙述错误的是( )
中的实际损耗,下列叙述错误的是( )
A.在FeO·FeyCrxO3中3x=y
B.![]() 反应中发生转移的电子的物质的量为3nx mol
反应中发生转移的电子的物质的量为3nx mol
C.处理废水中Cr2O72- 的物质的量为![]() mol
mol
D.消耗硫酸亚铁铵的物质的量为n(2—x)mol
D
本卷还有16题,登录并加入会员即可免费使用哦~

该作品由: 用户额鹅鹅鹅分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。