现有常温下的四种溶液:①0.01 mol/L的醋酸溶液 ②0.01 mol/L 的盐酸 ③pH=12的氨水 ④pH=12的NaOH溶液。下列说法正确的是( )
A.水的电离程度①中最小,③中最大
B.水的电离程度①中最大,②、③、④中相等
C.将②、③等体积混合,所得的溶液中由水电离出来的c(OH-)<1×10-7mol/L
D.将①、③等体积混合,所得的溶液中由水电离出来的c(OH-)>1×10-7mol/L
【答案】BC

常温下,某学生将0.1 mol·L-1 H2SO4溶液滴入0.1 mol·L-1 NaOH溶液,中和后加水至100 mL。若滴加过程中:①少滴了一滴H2SO4溶液;②多滴了一滴H2SO4溶液(1滴为0.05 mL),则①和②两种情况下所得溶液的pH之差是( )
A.4 B.4.6
C.5.4 D.6
【答案】D

25 ℃时,Kw=1×10-14;100 ℃时,Kw=1×10-12,下列说法正确的是( )
A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液恰好中和,所得溶液的pH=7
B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl溶液等体积混合,所得溶液的pH=7
C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L CH3COOH溶液恰好中和,所得溶液的pH=7
D.25 ℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH>7
【答案】D

一定物质的量浓度溶液的配制和酸碱中和滴定是化学中两个典型的定量实验。某研究性学习小组在实验室中配制1 mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中不正确的是( )
A.实验中所用到的滴定管、容量瓶,在使用前均需要检漏
B.如果实验中需用60 mL的稀硫酸标准溶液,配制时应选用 100 mL容量瓶
C.酸式滴定管用蒸馏水洗涤后,,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大
D.中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大
【答案】D
【解析】A项,滴定管、容量瓶使用前需检漏,正确;B项,实验室无60 mL容量瓶,选择容积比60 mL大而与之接近的容量瓶配制,B正确;C项,酸式滴定管不润洗使所测NaOH浓度偏大,正确;D项,导致实验结果偏小。
均值。一定要注意,数值相差太大的要舍弃。
下列图示与对应的叙述不相符合的是( )
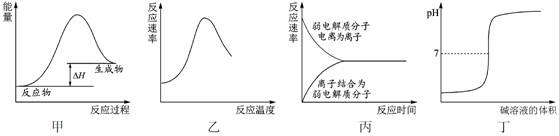
A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
【答案】A
【解析】燃烧为放热反应,反应物的总能量高于生成物的总能量,与图甲不符,A错误;反应开始温度升高,酶催化反应的反应速率加快,温度达到一定值,酶(蛋白质)发生变性,催化性能降低,反应速率变慢,B正确;将弱电解质加入水中,一开始弱电解质分子的电离速率大于离子结合成电解质分子的速率,随着电离的进行,二者速率相等,达到电离平衡,C正确;强碱滴定强酸的过程中溶液的pH逐渐增大,当接近滴定终点时pH发生突变,D正确。
本卷还有22题,登录并加入会员即可免费使用哦~

该作品由: 用户小小分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。