氨是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g)![]() 2NH3(g);△H= ―92.4kJ/mol他因此获得了1918年诺贝尔化学奖。试回答下列问题:
2NH3(g);△H= ―92.4kJ/mol他因此获得了1918年诺贝尔化学奖。试回答下列问题:
(1)合成氨工业中采取的下列措施可用勒夏特列原理解释的是 (填序号)
A、采用较高压强(20Mpa~50Mpa)
B、采用500℃的高温
C、用铁触媒作催化剂
D、将生成的氨液化并及时从体系中分离出来,N2和H2循环到合成塔中并补充N2和H2
(2)下图是实验室模拟工业法合成氨的简易装置。简述检验有氨气生成的方法 。
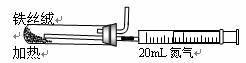
(3)在298K时,将10molN2和30molH2放入合成塔中,为何放出的热量小于924kJ? 。
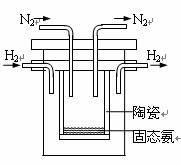
(4)1998年希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨。其实验装置如图。阴极的电极反应式 。
(1)A、D
(2)用湿润的红色石蕊试纸放到管口处,若变蓝说明有氨气生成。
(3)该反应是可逆反应,10molN2和30molH2不可能完全反应,所以放出的热量小于924kJ。
(4)N2+6 H++6e-=2NH3
CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是 。
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30 倍,CH4完全燃烧反应的热化学方程式是: 。
(3)120℃、101 kPa下,a mL由CO、CH4组成的混合气体在bmL O2中完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应产生b mL CO2,则混合气体中CH4的体积分数为 (保留2位小数)。
②若燃烧后气体体积缩小了a/4 mL ,则a与b关系的数学表示式是 。
(1)1:4
(2)CH4(g) + 2O2(g) == CO2(g) + 2H2O(l);△H = -891KJ/mol
(3)① 0.33② b≥5a/4
将4 mol SO3气和4 mol NO置于2 L容器中,一定条件下发生如下可逆反应(不考虑NO2和N2O4之间的相互转化): 2SO3(g) ![]() 2SO2+O2 2NO+O2
2SO2+O2 2NO+O2 ![]() 2NO2
2NO2
(1)当上述系统达到平衡时,O2和NO2的物质的量分别为n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO3气体的物质的量为 。
(2)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是SO3和 ,或NO和 (填它们的分子式)。
(3)若在另外一个2 L的容器中只发生反应2NO+O2 ![]() 2NO2,其中NO、O2、NO2的起始浓度依次是0.2 mol/L、0.1 mol/L、0.2 mol/L,当反应达到平衡时,各物质的浓度可能是 (填字母代号) 。
2NO2,其中NO、O2、NO2的起始浓度依次是0.2 mol/L、0.1 mol/L、0.2 mol/L,当反应达到平衡时,各物质的浓度可能是 (填字母代号) 。
A、c(NO)=0.35 mol/L或c(NO)=0.09 mol/L
B、c(NO2)=0.4 mol/L
C、c(NO2)=0.35 mol/L
D、c(O2)=0.2 mol/L或c(NO)=0.4 mol/L
(1)0.2mol
(2)![]() 、
、![]()
(3)A、C

该作品由: 用户hzl5201314分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。