化学反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol中,已知H—H键能为436 kJ/mol,H—N键能为391 kJ/mol。则N≡N键的键能是 ( )
2NH3(g) ΔH=-92.4 kJ/mol中,已知H—H键能为436 kJ/mol,H—N键能为391 kJ/mol。则N≡N键的键能是 ( )
A.431 kJ/mol B.946 kJ/mol C.649 kJ/mol D.869 kJ/mol
B
恒温下,反应aX(g) ![]() bY(g)+cZ(g)达到平衡,把容器体积压缩至原来的1/2,且达到新平衡时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L,下列判断正确的是
bY(g)+cZ(g)达到平衡,把容器体积压缩至原来的1/2,且达到新平衡时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L,下列判断正确的是
A.a>b+c B.a<b+c C.a=b+c D.a=b=c
A
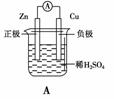
关于如图所示装置的叙述,正确的是 ( )
A.铜是阳极,铜片上有气泡产生
B.铜片附近的SO![]() 离子浓度逐渐增大
离子浓度逐渐增大
C.经导线,电流从锌流向铜,电子由铜流向锌
D.氢离子在铜片表面被还原,铜片上有H2逸出
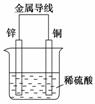
D
分析下列反应在任何温度下均能自发进行的是 ( )
A.2N2(g)+O2(g) === 2N2O(g) ΔH=+163 kJ·mol-1
B.2Ag(s)+Cl2(g) === 2AgCl(s) ΔH=-254 kJ·mol-1
C.2HgO(s) === 2Hg(l)+O2(g) ΔH=+182 kJ·mol-1
D.2H2O2(l) === O2(g)+2H2O(l) ΔH=-196 kJ·mol-1
D
本卷还有19题,登录并加入会员即可免费使用哦~

该作品由: 用户wei分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。