2018 年是门捷列夫诞辰 184 周年。下列事实用元素周期律不能解释的是
A . 沸点: H 2 O>H 2 S B . 碱性: KOH>NaOH
C . 酸性: HClO 4 >H 2 SO 4 D . 元素的金属性: Mg>Al
A
【分析】
根据元素周期律的定义:元素的某些性质随着原子序数的递增呈现周期性的变化,而递变的性质有元素的金属性和非金属性,最高价氧化物水化物的酸性和碱性等 , 据此判断 选项。
【详解】
A .由于水分子之间存在氢键,而硫化氢分子没有氢键,沸点大小为 H 2 O>H 2 S ,但这种解释不是周期律,故 A 符合题意;
B .根据金属性越强,元素最高价氧化物对应水化物碱性越强,钾和钠位于同一主族,从上到下金属性增强,故碱性: KOH>NaOH ,符合元素周期律,故 B 不符合题意;
C .根据非金属性越强,元素最高价氧化物对应水化物酸性越强, Cl 和 S 位于同一周期,从左到右非金属增强,故非金属性 Cl>S ,酸性: HClO 4 >H 2 SO 4 ,故 C 不符合题意;
D .元素的金属性,同周期中从左到右逐渐减弱, D 符合元素周期律,故 D 不符合题意;
故选答案 A 。
【点睛】
注意物质沸点的比较根据物质所属晶体类型进行判断,而元素周期律中晶体的类型没有递变规律。
下列各组微粒不是按半径逐渐增大的顺序排列的是
A . Na 、 K 、 Rb B . F 、 Cl 、 Br C . Mg 2+ 、 Al 3+ 、 Zn 2+ D . Cl - 、 Br - 、 I -
C
【详解】
A .同主族元素,从上到下,原子半径 ( 离子半径 ) 逐渐增大,则 Na 、 K 、 Rb 原子半径逐渐增大, A 不符题意;
B .同主族元素,从上到下,原子半径 ( 离子半径 ) 逐渐增大,则 F 、 Cl 、 Br 原子半径逐渐增大, B 不符题意;
C . Zn 2+ 电子层数最多,半径最大, Mg 2+ 、 Al 3+ 电子层数相同但 Al 的核电荷数大,所以 Al 3+ 的半径小与 Mg 2+ , C 符合题意;
D .同主族元素,从上到下,原子半径 ( 离子半径 ) 逐渐增大,则 Cl - 、 Br - 、 I - 半径逐渐增大, D 不符题意;
答案选 C 。
有 X、Y、Z三种元素,它们的原子序数都小于20,对应离子X + 、 Y 2- 、 Z - 具有相同的电子层结构。有关描述中正确的是
A . 原子序数: Z>X>Y B . 还原性: Z - >Y 2-
C . Z元素最高价为+7 D . X与Y可形成X 2 Y 2 化合物
D
【分析】
X 、 Y 、 Z 三种元素,它们的原子序数都小于 20 ,对应离子 X + 、 Y 2- 、 Z - 具有相同的电子层结构。 X 失去 1 个电子被氧化成 X + ; Y 得到 2 个电子被还原成 Y 2- ;为 Z 得到 1 个电子被还原成 Z - ,所以 X 、 Y 、 Z 三种元素的原子序数大小为 X > Z > Y 。 Y 、 Z 同周期,且 Z 的非金属性强于 Y , X 为金属。据此分析可得。
【详解】
A.由分析可知,原子序数X>Z>Y,故A错;
B.由分析可知,Z的非金属性强于Y,则还原性:Z - < Y 2- ,故 B错;
C.Z为原子序数小于20的元素,其的最低负价为-1价,X + 、 Y 2- 、 Z - 具有相同的电子层结构,则 Z可能为F或者Cl,当Z为F时无正价,故C错;
D.若X为Na、Y为O时,则X与Y可形成X 2 Y 2 即 Na 2 O 2 化合物,故选 D;
答案选 D。
短周期主族元素 X 、 Y 、 Z 、 W 的原子序数依次增大,它们原子的最外层电子数之和为 16 , Y 的单质是空气中含量最多的气体, Z 原子的最外层电子数是其内层电子数的 3 倍, W 是短周期中金属性最强的元素。下列说法正确的是
A . X 最高价氧化物对应的水化物为强酸 B . 原子半径: r (W) > r (X) > r (Y) > r (Z)
C . X 、 Y 、 Z 的非金属性依次减弱 D . 由 Z 和 W 组成的化合物只有一种
B
【分析】
短周期主族元素 X 、 Y 、 Z 、 W 的原子序数依次增大, Y 的单质是空气中含量最多的气体,则 Y 为 N 元素; Z 原子的最外层电子数是其内层电子数的 3 倍,则内层电子数为 2 ,最外层电子数为 6 , Z 为 O 元素; W 是短周期中金属性最强的元素,则 W 是 Na 元素;它们原子的最外层电子数之和为 16 , X 最外层电子数 =16-5-6-1=4 ,则 X 为 C 元素,据此分析解答。
【详解】
根据上述分析, X 为 C 元素, Y 为 N 元素, Z 为 O 元素, W 为 Na 元素。
A . X 为 C 元素, X 最高价氧化物对应的水化物 H 2 CO 3 为弱酸,选项 A 错误;
B .一般而言,电子层数越多,原子半径越大;同一周期,原子半径随着原子序数增大而减小,因此原子半径: r (W) > r (X) > r (Y) > r (Z) ,选项 B 正确;
C .同一周期,元素的非金属性随着原子序数增大而增强,非金属性 X 、 Y 、 Z 依次增强,则 X 、 Y 、 Z 的气态氢化物稳定性依次增强,选项 C 错误;
D .由 Z 和 W 组成的化合物有 Na 2 O 、 Na 2 O 2 ,选项 D 错误;
答案选 B 。
如图为元素周期表的一部分, X 、 Y 、 Z 、 W 均为短周期元素,若 Z 原子最外层电子数是次外层电子数的 。则下列说法正确的是
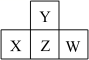
A . X 、 Y 二种元素都仅能形成一种单质
B . X 与 O 2 反应的产物可作为干燥 NH 3 的干燥剂
C . Z 的氧化物中有一种是形成酸雨的主要物质
D . W 不能形成含氧酸
C
【分析】
X 、 Y 、 Z 、 W 均为短周期元素,若 Z 原子最外层电子数是次外层电子数的 ,则 Z 为 S , Y 为 O , X 为 P , W 为 Cl 。
【详解】
由以上分析可知 X 是 P 元素, Y 是 O 元素, Z 是 S 元素, W 是 Cl 元素,
A . P 形成的单质有白磷、红磷, O 形成的单质有氧气、臭氧,故 A 错误;
B . P 2 O 5 可以作干燥剂,但是酸性氧化物,与氨气反应,不能干燥氨气,故 B 错误;
C . Z 为硫,氧化物有二氧化硫、三氧化硫,二氧化硫是形成酸雨的主要物质,故 C 正确;
D . W 是 Cl ,可以形成次氯酸、高氯酸等含氧酸,故 D 错误。
故选 C 。
本卷还有45题,登录并加入会员即可免费使用哦~

该作品由: 用户李杰分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。