用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 60 g甲醛和乙酸的混合物中所含碳原子数为2NA
B. 0.5mol C3H8分子中所含C-C共价键数为1.5NA
C. 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为![]() NA
NA
D. 1mol碳正离子CH5+ 所含的电子数为11NA
【答案】A
【解析】
【详解】A.甲醛HCHO和乙酸CH3COOH的最简式均为CH2O,故60g混合物中含有的CH2O的物质的量为n=![]() =2mol,含2mol碳原子,即2NA个碳原子,故A正确;
=2mol,含2mol碳原子,即2NA个碳原子,故A正确;
B.一个丙烷分子中含2条C-C键,故0.5mol丙烷中含NA条C-C共价键,故B错误;
C.标准状况下,庚烷为液体,不能根据气体摩尔体积来计算其物质的量和生成的分子数,故C错误;
D.一个CH5+含10个电子,1mol碳正离子中含电子10NA个,故D错误;
答案选A。
下列事实、离子方程式及其对应关系均正确的是( )
A. 铁溶于稀硝酸,溶液变为浅绿色:Fe+4H++NO3-=== Fe3++NO↑+2H2O
B. 向K2Cr2O7溶液中滴加少量浓H2SO4,溶液变为黄色:Cr2O72-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
C. 向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I+O2 === 2I2+2H2O
D. 向水杨酸(![]() )中滴加NaHCO3溶液,放出无色气体:
)中滴加NaHCO3溶液,放出无色气体:![]() +2HCO3-
+2HCO3-![]()
![]() +2CO2↑+2H2O
+2CO2↑+2H2O
【答案】C
【解析】
试题分析:A、少量铁粉溶于稀硝酸Fe+4HNO3=Fe(NO3)3+NO(气体)+2H2O,溶液显黄色;过量铁粉溶液稀硝酸3Fe+8HNO3=3Fe(NO3)2+2NO(气体)+4H2O溶液显浅绿色,故A错误;B、加酸后平衡逆向移动,溶液显红色;C、淀粉碘化钾在酸溶液中被氧化生成碘单质,溶液变蓝,故C正确;D、![]() + HCO3- →
+ HCO3- →![]() H+ CO2↑ + H2O
H+ CO2↑ + H2O
考点:离子反应方程式的书写;
常温下,分别用0.1 mol·L1溶液进行下列实验,结论不正确的是( )
A. 向NaHCO3溶液中通CO2至pH=7:c(Na+) = c(HCO3-) +2c(CO32-)
B. 向CH3COONa溶液中加入等浓度等体积的盐酸:c(Na+)=c(Cl)
C. 向NaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH=13
D. 向氨水中加入少量NH4Cl固体:![]() 增大
增大
【答案】C
【解析】
试题分析:A.溶液呈电中性,根据电荷守恒c(Na+)+c(H+) = c(HCO![]() ) +2c(CO
) +2c(CO![]() )+c(OH-),室温下溶液的pH=7为中性,c(H+)=c(OH-),所以c(Na+) = c(HCO3-) +2c(CO32-),A项正确;B.因为溶液等体积等浓度,则可推出混合溶液后的不水解的c(Na+)和c(Cl
)+c(OH-),室温下溶液的pH=7为中性,c(H+)=c(OH-),所以c(Na+) = c(HCO3-) +2c(CO32-),A项正确;B.因为溶液等体积等浓度,则可推出混合溶液后的不水解的c(Na+)和c(Cl![]() )相等,B项正确;C.设体积为1L,则向0.1mol/L的NaHSO4溶液中加入0.1mol/L的Ba(OH)2溶液1L,反应后c(OH-)=(0.2-0.1)÷2=0.05mol/L,pH≠13,C项错误;D.氨水中存在NH3•H2O
)相等,B项正确;C.设体积为1L,则向0.1mol/L的NaHSO4溶液中加入0.1mol/L的Ba(OH)2溶液1L,反应后c(OH-)=(0.2-0.1)÷2=0.05mol/L,pH≠13,C项错误;D.氨水中存在NH3•H2O![]() NH4++OH-,加入少量NH4Cl固体相当于加入NH4+,平衡逆向移动,但移动是微弱的过程,则
NH4++OH-,加入少量NH4Cl固体相当于加入NH4+,平衡逆向移动,但移动是微弱的过程,则![]() 增大,D项正确;答案选C。
增大,D项正确;答案选C。
考点:考查离子浓度的大小比较,溶液的酸碱性与pH值,弱电解质的电离等知识。
如图所示,下列说法正确的是( )
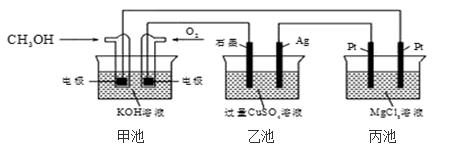
A. 若将乙池电解液换成 AgNO3 溶液,则可以实现在石墨棒上镀银
B. 甲池通入 CH3OH 的电极反应式为 CH3OH+6e+2H2O═CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量 Cu(OH)2 固体,能使 CuSO4 溶液恢复到原浓度
D. 甲池中消耗 224mL(标准状况下)O2,此时丙池中理论上产生 1.16g 固体
【答案】D
【解析】
【分析】
根据图示,甲池为原电池,通入甲醇的为负极,则乙池中银电极和丙池中右边的铂电极为阴极;通入氧气的为正极,则乙池中石墨电极和丙池中左边的铂电极为阳极,据此分析解答。
【详解】A.乙池中石墨连接甲池的正极,为电解池的阳极,银电极为阴极,若将乙池电解液换成 AgNO3 溶液,阳极上溶液中的氢氧根离子放电生成氧气,不能实现在石墨棒上镀银,故A错误;
B.在燃料电池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为CH3OH-6e-+2H2O+8OH-=CO32-+8H2O,故B错误;
C.电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,不能加入氢氧化铜,故C错误;
D.甲池中消耗224mL(标准状况下)O2,即![]() =0.01mol,转移电子0.04mol,根据转移的电子守恒,丙池中生成0.02mol氢气,同时生成0.04mol氢氧根离子,氢氧根离子和镁离子生成氢氧化镁沉淀,所以氢氧化镁沉淀的物质的量是0.02mol,氢氧化镁沉淀的质量=0.02mol×58g/mol=1.16g,故D正确;
=0.01mol,转移电子0.04mol,根据转移的电子守恒,丙池中生成0.02mol氢气,同时生成0.04mol氢氧根离子,氢氧根离子和镁离子生成氢氧化镁沉淀,所以氢氧化镁沉淀的物质的量是0.02mol,氢氧化镁沉淀的质量=0.02mol×58g/mol=1.16g,故D正确;
答案选D。
【点睛】正确判断装置图中各装置的作用是解题的关键。本题的易错点为B,要注意书写电极反应式时要结合电解质溶液的酸碱性,电解质溶液不同电极反应式不同。
大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物光化学烟雾,其中某些反应过程如图所示。下列说法正确的是( )

A. 丙烯发生氧化反应生成甲醛和乙醛
B. 生成O3的反应属于氧化还原反应
C. 反应 I 属于复分解反应
D. 该过程中O2作催化剂
【答案】A
【解析】
A、丙烯转化成甲醛和乙醛,是丙烯中的双键发生断裂,此反应属于氧化反应,故A正确;B、根据示意图,O2→O3,化合价没有发生变化,因此生成O3的反应不属于氧化还原反应,故B错误;C、反应I中NO转化成NO2,化合价升高,即反应I为氧化还原反应,故C错误;D、有O2参与反应,但后面没有O2的生成,因此O2不作催化剂,故D错误。
本卷还有15题,登录并加入会员即可免费使用哦~

该作品由: 用户LS分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。