下列叙述正确的是( )
A.漂白粉、水玻璃、冰醋酸、聚乙烯都是混合物
B.金属氧化物一定是碱性氧化物
C.胶体区别于其他分散系的本质特征是胶体粒子直径介于1~100 nm之间
D.淀粉、油脂和蛋白质都属于天然高分子化合物
C
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓硝酸或浓硫酸反应生成SeO2以回收Se。
完成下列填空:
(1)Se与浓硝酸反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1∶1,写出Se与浓硝酸反应的化学方程式: 。
(2)已知:Se+2H2SO4(浓)![]() 2SO2↑+SeO2+2H2O
2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O![]() Se+2S
Se+2S![]() +4H+
+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是 。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3![]() Se+I2+KNO3+H2O
Se+I2+KNO3+H2O
②I2+2Na2S2O3![]() Na2S4O6+2NaI
Na2S4O6+2NaI
配平方程式①,标出电子转移的方向和数目: 。
(4)实验中,准确称量SeO2样品0.150 0 g,消耗了0.200 0 mol·L-1的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为 。
答案 (1)Se+2HNO3(浓)![]() H2O+SeO2+NO↑+NO2↑
H2O+SeO2+NO↑+NO2↑
(2)H2SO4(浓)>SeO2>SO2
(3)![]()
(4)92.50%(或0.925 0)
工业上可用以下方案使饮用水中N![]() 含量达标。
含量达标。
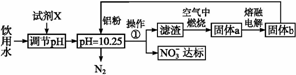
请回答下列问题:
(1)调节pH不宜过大或过小,否则会造成 的利用率降低;试剂X可选用 (填序号)。
A.NaOH B.Ca(OH)2 C.NH3·H2O D.CuO E.CO2
(2)流程中操作①的名称为 ,若在实验室中进行此操作,所需要的玻璃仪器是 。
(3)写出溶液中铝粉和N![]() 反应的离子方程式: 。
反应的离子方程式: 。
(4)还可用以下化学反应使饮用水中N![]() 的含量达标,产物之一是空气的主要成分。完成下列离子方程式:
的含量达标,产物之一是空气的主要成分。完成下列离子方程式:
H2+ N![]() +
+ ![]()
+ H2O
答案 (1)铝 B
(2)过滤 烧杯、漏斗、玻璃棒
(3)10Al+6N![]() +18H2O
+18H2O![]() 10Al(OH)3+3N2↑+6OH-
10Al(OH)3+3N2↑+6OH-
(4)5H2+2N![]() +2H+
+2H+![]() N2+6H2O
N2+6H2O
下列我国古代的技术应用中,其工作原理不涉及化学反应的是( )
| A.火药使用 | B.粮食酿酒 | C.转轮排字 | D.铁的冶炼 |
|
|
|
|
|
C
向含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol的混合溶液中加入0.1 mol Fe粉,充分搅拌后Fe粉溶解,溶液中不存在Fe3+,同时析出0.1 mol Ag。下列结论错误的是( )
A.氧化性:Zn2+>Cu2+>Fe3+>Ag+
B.Fe3+的氧化性强于Cu2+
C.溶液中Cu2+与Fe2+的物质的量之比为1∶2
D.1 mol Fe可还原2 mol Fe3+
A
本卷还有9题,登录并加入会员即可免费使用哦~

该作品由: 用户小小分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。

