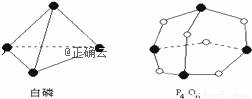
 已知白磷和P4O6的分子结构如图,现提供以下化学键的键能: P-P:198 kJ·mol-1 P-O:360 kJ·mol-1 O=O:498 kJ·mol-1,则反应P4(白磷)+3O2=P4O6的反应热△H为( )
已知白磷和P4O6的分子结构如图,现提供以下化学键的键能: P-P:198 kJ·mol-1 P-O:360 kJ·mol-1 O=O:498 kJ·mol-1,则反应P4(白磷)+3O2=P4O6的反应热△H为( )
A.-126 kJ·mol-1
B.-1638 kJ·mol-1
C.+126 kJ·mol-1
D.+1638 kJ·mol-1
B
下列反应的离子方程式表达正确的是( )
A.FeCl3溶液中滴加HI溶液:2Fe3++2HI===2Fe2++2H++I2
B.1 mol·L-1 NaAlO2溶液和4 mol·L-1 HCl溶液等体积混合:AlO![]() +4H+===Al3++2H2O
+4H+===Al3++2H2O
C.NH4HSO4溶液中滴加少量Ba(OH)2溶液:
NH![]() +H++SO
+H++SO![]() +Ba2++ 2OH-===BaSO4↓+NH3·H2O+H2O
+Ba2++ 2OH-===BaSO4↓+NH3·H2O+H2O
D.Na2S2O3溶液中滴加过量稀H2SO4:3S2O![]() +2H+===4S↓+2SO
+2H+===4S↓+2SO![]() +H2O
+H2O
B
已知:2H2(g)+O2(g)![]() 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)![]() H2O(l) ΔH=-57.3 kJ·mol-1
H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是( )
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.H2SO4(aq)+Ba(OH)2(aq)![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
C.3H2(g)+CO2(g)![]() CH3OH(l) +H2O(l) ΔH=+135.9 kJ·mol-1
CH3OH(l) +H2O(l) ΔH=+135.9 kJ·mol-1
D.等质量的H2(g)和CH3OH(l)完全燃烧,H2(g)燃烧放出的热量多
D
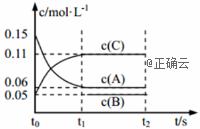
向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体,一定条件下发生如下反应: 3A(g) ![]() B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1阶段的 c(B)变化未画出]。下列说法中正确的是( )
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1阶段的 c(B)变化未画出]。下列说法中正确的是( )
A.若 t1=15 s,则用 A 的浓度变化表示 t0~t1阶段的 平均反应速率为 0.004 mol·L-1·s-1
B.该容器的容积为2 L,B的起始的物质的量为 0.02 mol
C. t1时该反应达到平衡,A的转化率为 60%
D. t0~t1阶段,此过程中容器与外界的热交换总量为 a kJ,该反应的热化学方程式为
3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
C
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) ![]() 2CO2(g)+S(l) ΔH<0。一定温度下,在容积为2 L的恒容密闭容器中1 mol SO2和n mol CO发生反应,5 min后达到平衡,生成2a mol CO2。下列说法正确的是( )
2CO2(g)+S(l) ΔH<0。一定温度下,在容积为2 L的恒容密闭容器中1 mol SO2和n mol CO发生反应,5 min后达到平衡,生成2a mol CO2。下列说法正确的是( )
A.反应前2 min的平均速率v(SO2)=0.1a mol·L-1·min-1
B.平衡后保持其他条件不变,从容器中分离出部分硫,平衡向正反应方向移动
C.平衡后保持其他条件不变,升高温度和加入催化剂,SO2的转化率均增大
D.当混合气体的物质的量不再改变时,反应达到平衡状态
D
本卷还有16题,登录并加入会员即可免费使用哦~

该作品由: 用户辛雨分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。