设NA为阿伏加徳罗常数的值,下列说法正确的是 ( )
A. 1LpH=2的硫酸溶液中SO42-数目等于0.01NA
B. 室温下,pH=6的NH4Cl溶液中,由水电离的H+浓度为10-6mol/L
C. 常温下,1mol/L盐酸溶液中H+个数等于0.1NA
D. 在密闭容器内充入0.50molNO和0.25molO2,充分反应后容器内分子数为0.5NA
【答案】B

设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 6g SiO2晶体中含有Si-O键的数目为0.2NA
B. 1mol乙酸与足量的乙醇发生酯化反应,生成乙酸乙酯分子数为NA个
C. 某温度下, pH=2的H2SO4溶液中,硫酸和水电离的H+总数为0.01NA
D. 常温下,1L 0.1mol·L-1醋酸钠溶液中加入醋酸至溶液为中性,则溶液含醋酸根离子数0.1NA个
【答案】D
【解析】A项, 1molSiO2晶体中含有Si-O键的数目为4NA,所以6g(即0.1mol)SiO2晶体中含有Si-O键的数目为0.4NA,故A错误;B项,乙酸与乙醇生成乙酸乙酯是可逆反应,所以1mol乙酸与足量的乙醇发生酯化反应,生成乙酸乙酯分子数小于NA个,故B错误;C项,某温度下,pH=2的H2SO4溶液中,c(H+)=0.01mol/L,溶液体积未知,无法求得H+总数,故C错误;D项,醋酸钠溶液中加入醋酸至溶液为中性,根据电荷守恒得:醋酸根离子与钠离子浓度相等,所以溶液含醋酸根离子物质的量为:1L×0.1mol·L-1=0.1mol,即0.1NA个,故D正确。
下列事实与水解反应无关的是
A. 用Na2S除去废水中的Hg2+ B. 用热的Na2CO3溶液去油污
C. 利用油脂的皂化反应制造肥皂 D. 配制CuSO4溶液时加少量稀H2SO4
【答案】A

向FeCl3溶液中加入Na2SO3溶液,测定混合后溶液pH随混合前溶液中c(SO32-)/c(Fe3+)变化的曲线如图所示。实验发现:
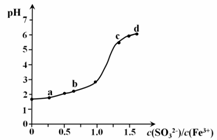
i. a点溶液透明澄清,向其中滴加NaOH溶液后,立即产生灰白色沉淀,滴入KSCN溶液显红色;
ii. c点和d点溶液中产生红褐色沉淀,无气体逸出。取其上层清液滴加NaOH溶液后无明显现象,滴加KSCN溶液显红色。下列分析合理的是
A. 向a点溶液中滴加BaCl2溶液,无明显现象
B. b点较a点溶液pH升高的主要原因:2Fe3+ + SO32- + H2O === 2Fe2+ + SO42- + 2H+
C. c点溶液中发生的主要反应:2Fe3+ + 3SO32- + 6H2O![]() 2Fe(OH)3↓+ 3H2SO3
2Fe(OH)3↓+ 3H2SO3
D. 向d点上层清液中滴加KSCN溶液,溶液变红;再滴加NaOH溶液,红色加深
【答案】C
【解析】A.由以上分析得,向a点溶液中滴加BaCl2溶液,有硫酸钡白色沉淀产生,故A错误;B.若2Fe3++SO32-+H2O═2Fe2++SO42-+2H+,发生此反应,酸性加强,pH减小,故B错误;C.c点和d点溶液中产生红褐色沉淀,无气体逸出,故发生的反应为2Fe3++3SO32-+6H2O⇌2Fe( OH)3+3H2SO3,故C正确;D.d点发生的反应为2Fe3++3SO32-+6H2O⇌2Fe( OH)3↓+3H2SO3,这是一个可逆反应,反应物不能完全转化为生成物,故滴加KSCN溶液,溶液变红;滴加NaOH溶液,平衡向正反应方向移动,铁离子浓度减少,红色变浅,故D错误;故选C。
下列溶液配制实验的描述完全正确的是
A. 在实验室,学生一般无需查阅资料即可用一定体积75%的硝酸来配制250 mL 2 mol·L-1的硝酸溶液
B. 实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中再加水稀释
C. 用浓盐酸配制1∶1(体积比)的稀盐酸(约 6 mol·L-1)可以直接在容量瓶中配制
D. 用pH=1的盐酸配制100 mL pH=2的盐酸所需全部玻璃仪器有100 mL容量瓶、烧杯、玻璃棒、胶头滴管
【答案】B

本卷还有27题,登录并加入会员即可免费使用哦~

该作品由: 用户菲的天堂分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。