下列说法正确的是( )
①电解是把电能转变成化学能的过程 ②电解是化学能转变成电能的过程 ③电解质溶液导电是化学变化,金属导电是物理变化 ④不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤任何溶液被电解时,必然导致氧化还原反应的发生
A.①②③④ B.②③⑤
C.③④ D.①③④⑤
解析:选D。从能量角度看,电解是把电能转变成化学能的过程,故①对、②错;电解质溶液的导电过程,必将伴随着两个电极上氧化还原反应的发生,同时生成新的物质,故③、⑤对;某些不能自发进行的氧化还原反应,通过电解的原理供给电能也可以实现,故④对。所以D选项符合题意。
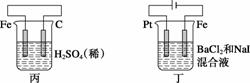
有关甲、乙、丙、丁四个图示的叙述正确的是( )
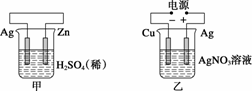
A.甲中负极反应式为2H++2e-===H2↑
B.乙中阳极反应式为Ag++e-===Ag
C.丙中H+向碳棒方向移动
D.丁中电解开始时阳极产生黄绿色气体
解析:选C。由图可知,甲、丙是原电池,甲中Zn为负极,电极反应为Zn-2e-=== Zn2+,A项错误;丙中Fe为负极,碳棒为正极,H+向碳棒方向移动,C项正确;乙、丁为电解池,乙中Ag为阳极,自身失去电子,B项错误;丁中放电顺序为I->Cl-,开始时阳极产生碘单质,阴极产生H2,D项错误。
为使反应Cu+2H2O===Cu(OH)2↓+H2↑能够发生,下列设计方案正确的是( )
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
解析:选C。该反应为不能自发进行的氧化还原反应,必须设计为电解池才能发生。阳极为Cu放电,阴极为H+放电,即用Cu作阳极,电解质溶液中为H2O放电,选项C符合要求。
如图所示,下列叙述正确的是( )
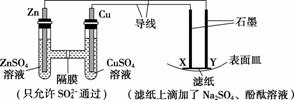
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
解析:选A。从题图中可以看出,左边的装置为原电池而右边的装置为电解池。根据原电池原理,较活泼的一极作原电池的负极,所以Zn为负极,Cu为正极。再根据电解原理,Y与Zn片相连为阴极,X与Cu片相连为阳极,Y极的电极反应式为2H++2e-===H2↑(还原反应);X极的电极反应式为4OH--4e-===2H2O+O2↑(氧化反应)。Y极上H+放电,同时产生了OH-,呈碱性,使酚酞溶液呈红色。
将含有KCl、CuBr2、Na2SO4三种物质的水溶液用铂电极进行电解,且电解时间足够长。有以下结论:①溶液中几乎没有Br-;②电解质溶液为无色;③最终溶液显碱性;④K+、Na+和SO![]() 的浓度几乎没有变化。正确的是(设Cl2、Br2全部从溶液中逸出)( )
的浓度几乎没有变化。正确的是(设Cl2、Br2全部从溶液中逸出)( )
A.①②③ B.③
C.①④ D.均正确
解析:选A。溶液中存在的阴离子有Cl-、Br-、SO![]() 、OH-,阳离子有K+、Cu2+、Na+、H+。因用Pt电极电解足够长的时间,阴离子首先放电的是Br-,其次是Cl-,最后是OH-,SO
、OH-,阳离子有K+、Cu2+、Na+、H+。因用Pt电极电解足够长的时间,阴离子首先放电的是Br-,其次是Cl-,最后是OH-,SO![]() 在溶液中不放电,阳离子首先放电的是Cu2+,其次是H+。所以先电解CuBr2,阳极逸出Br2,阴极析出Cu。CuBr2消耗完后继续电解HCl(H+来自于水中)。当Cl-被消耗尽时,则继续电解水。由于水被消耗,c(K+)、c(Na+)和c(SO
在溶液中不放电,阳离子首先放电的是Cu2+,其次是H+。所以先电解CuBr2,阳极逸出Br2,阴极析出Cu。CuBr2消耗完后继续电解HCl(H+来自于水中)。当Cl-被消耗尽时,则继续电解水。由于水被消耗,c(K+)、c(Na+)和c(SO![]() )会增大。
)会增大。
本卷还有8题,登录并加入会员即可免费使用哦~

该作品由: 用户陈建平分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。