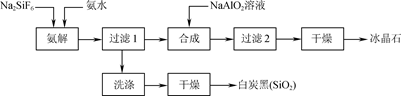
使用磷肥副产物氟硅酸钠(Na2SiF6)为原料合成冰晶石(Na3AlF6)成为一条合理利用资源、提高经济效益的新方法。工艺流程如下图所示:

(1)传统合成冰晶石的方法是萤石(CaF2)法:使用萤石、石英和纯碱在高温下煅烧生成NaF,在NaF溶液中加入Al2(SO4)3溶液制得。在加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,


否则可能产生副产物____(填物质的化学式),但酸度不宜过强的原因是____。
(2)氨解时白炭黑产率和冰晶石纯度与pH的关系如图,氨解时需要控制溶液的pH=____;能提高氨解速率的措施有____(填字母)。
A.快速搅拌
B.加热混合液至100℃
C.减小氨水浓度
(3)工艺流程中氨解反应的化学方程式为____;冰晶石合成反应的离子方程式为______。
(4)为了提高原料利用率,减少环境污染,可采取的措施是___。
答案
【答案】Al(OH)3 H+和F-结合生成弱酸HF,使F-浓度减低不易生成Na3AlF6 8.5 A Na2SiF6+4NH3·H2O=2NaF+4NH4F+SiO2↓+2H2O 3Na++4NH4++6F-+AlO2-+2H2O=Na3AlF6↓+4NH3·H2O 过滤2的滤液氨水可循环利用
【解析】 (1)传统合成冰晶石的方法是萤石(CaF2)法,是使用萤石、石英和纯碱在高温下煅烧生成NaF,在NaF溶液中加入Al2(SO4)3溶液制得。NaF水解,溶液显碱性,在加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,防止加入硫酸铝后生成Al(OH)3沉淀;但酸度不宜过强,否则H+和F-结合生成弱酸HF,使F-浓度减低不易生成Na3AlF6,故答案为:Al(OH)3;H+和F-结合生成弱酸HF,使F-浓度减低不易生成Na3AlF6;
(2)从图可知,pH为8.5时,冰晶石中白炭黑的含量较低,冰晶石纯度较高,白炭黑产率高;A.快速搅拌可以加快反应速率,故A正确;B.加热混合液至100℃,氨水受热分解,反应物浓度小,化学反应速率减慢,故B错误;C.减小氨水浓度,化学反应速率减慢,故C错误;故答案为:8.5;A;
(3) 根据流程图,氨水浸取氟硅酸钠时生成了二氧化硅,则同时会生成NaF、NH4F和H2O,反应的方程式可以表示为Na2SiF6+4NH3•H2O═2NaF+4NH4F+ SiO2↓+2H2O,水浴加热过程中生成冰晶石的化学方程式为:2NaF+4NH4F+NaAlO2+2H2O= Na3AlF6↓+4NH3·H2O,离子方程式为3Na++4NH4++6F-+AlO2-+2H2O=Na3AlF6↓+4NH3·H2O,故答案为:Na2SiF6+4NH3•H2O═2NaF+4NH4F+ SiO2↓+2H2O;3Na++4NH4++6F-+AlO2-+2H2O=Na3AlF6↓+4NH3·H2O;
(4)根据上述分析,第二次过滤所得滤液为氨水溶液,为了提高原料利用率,减少环境污染,可循环使用氨水,故答案为:过滤2的滤液氨水可循环利用。

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L